
| A.该合金中铜与镁的物质的量之比是2?1 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
| C.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
| D.NO2和N2O4的混合气体中,NO2的体积分数是80% |
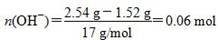 ,故2x+2y=0.06 mol ②,由①②解得x=0.02 mol,y=0.01 mol,显然A正确。
,故2x+2y=0.06 mol ②,由①②解得x=0.02 mol,y=0.01 mol,显然A正确。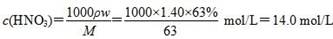 ,B正确。得到2.54 g沉淀时,消耗0.06 mol NaOH,其体积为60 mL,C错误。由上述分析可知,Cu、Mg共失去0.06 mol电子,根据得失电子守恒知,如果硝酸完全被还原为NO2,NO2的物质的量应为0.06 mol。现得到0.05 mol混合气体,是由于2NO2??N2O4,由差量法可求得N2O4为0.01 mol,则NO2为0.04 mol,显然D正确。
,B正确。得到2.54 g沉淀时,消耗0.06 mol NaOH,其体积为60 mL,C错误。由上述分析可知,Cu、Mg共失去0.06 mol电子,根据得失电子守恒知,如果硝酸完全被还原为NO2,NO2的物质的量应为0.06 mol。现得到0.05 mol混合气体,是由于2NO2??N2O4,由差量法可求得N2O4为0.01 mol,则NO2为0.04 mol,显然D正确。

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:多选题
| A.Na2O2在反应中只作氧化剂 |
| B.O2是氧化产物 |
| C.Na2FeO4既是氧化产物又是还原产物 |
| D.2molFeSO4发生反应时,共有8mol电子转移 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成40.0LN2(标准状况) | B.有0.250molKNO3被氧化 |
| C.转移电子的物质的量为2.5mol | D.被氧化的N原子的物质的量为3.75mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.被氧化的砒霜为1.98mg |
| B.分解产生的氢气为0.672ml |
| C.和砒霜反应的锌为3.90mg |
| D.转移的电子总数为6×10―5NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
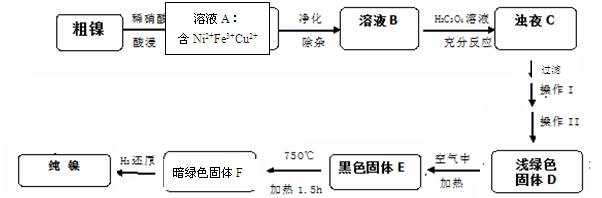
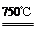 4NiO(暗绿色) + O2↑
4NiO(暗绿色) + O2↑| 物质 | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
| Ksp | 8.8×10-36 | 2.2×10-20 | 5.48×10-16 | 3.2×10-19 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu与Cu2O的物质的量之比为2∶1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2 mol | B.3 mol | C.4mol | D.5 mo1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com