
【题目】关于下列各装置图的叙述中,不正确的是( ) 
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.用装置①进行电镀,镀件接在b极上
C.装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+
D.装置③中的铁钉几乎没被腐蚀
科目:高中化学 来源: 题型:
【题目】下列有关碳酸盐溶液的说法中,不正确的是( )
A.在物质的量浓度相等的Na2CO3、NaHCO3两溶液中,阴离子总数相等
B.常温下,等物质的量浓度的Na2CO3溶液的pH大于NaHCO3溶液的pH
C.在NaHCO3溶液中一定有:c(Na+)>c(HCO![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
D.在Na2CO3溶液中一定有:c(Na+)+c(H+)=c(HCO![]() )+c(OH-)+2c(CO
)+c(OH-)+2c(CO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ag2SO4的Ksp 为2.0×10-5,将适量Ag2SO4固体溶于水中配成100 mL饱和溶液,该过程中Ag+和SO42-浓度随时间变化关系如图[饱和Ag2SO4溶液中c(Ag+)=0.034 mol·L-1]。若t1时刻在上述体系中加入100 mL 0.020 mol·L-1 Na2SO4 溶液,下列示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是( )
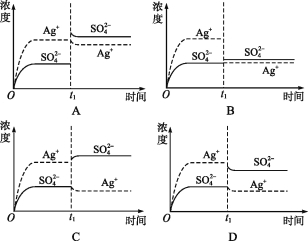
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种锂电池,用金属锂和石墨做电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯( ![]() )中而形成的,电池总反应方程式为:8Li+3SOCl2═6LiCl+Li2SO3+2S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为:8Li+3SOCl2═6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应 X+2Y = R+2M 中,已知R和M的摩尔质量之比为22:9,当1.6g X与Y完全反应后,生成4.4 g R, 则此反应中Y和M的质量之比为( )
A. 16:9 B. 23:9 C. 32:9 D. 46:9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( ) 
A.通电后中间隔室的SO42﹣离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2H2O﹣4e﹣=O2+4H+ , 负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)CH3OH(g)
(1)如表所列数据是该反应在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①该反应的熵变△S0 ( 填:“<,>,=”).该反应在(填:高温或低温)条件下能自发进行.
②要提高CO的转化率,可以采取的措施是(填序号).
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压
e.加入惰性气体加压 f.分离出甲醇
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率AC(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数AC,由状态B到状态A,可采用的方法(填“升温”或“降温”). 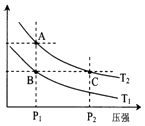
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于硝酸的认识,正确的是( )
A.浓硝酸和稀硝酸都具有强氧化性
B.铜和稀硝酸的反应属于置换反应
C.在铜与浓硝酸的反应中,硝酸只体现氧化性,没有体现酸性
D.可用铝或铁制容器盛装稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用元素周期律分析下面的推断正确的是
A. 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
B. 砹单质是一种有色固体,砹化氢很不稳定,砹化银是难溶于水的白色沉淀
C. 硫酸锶难溶于水,但易溶于盐酸
D. 硒化氢是无色、有毒、比硫化氢稳定的气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com