
【题目】某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如图: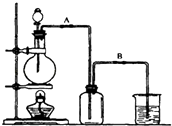
(1)实验开始前,某学生对装置进行了气密性检查.方法是:连接好装置后,用弹簧夹夹住处(填“A”或“B“)橡皮管;向分液漏斗中加水并打开活塞,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中时,表明该装置不漏气.
(2)上述反应中,若有4molHCl参加反应,转移的电子的物质的量是mol.
(3)若实验过程中看到集气瓶中有黄绿色液滴,说明氯气具有的性质是 .
【答案】
(1)B,液面高度不再变化
(2)2
(3)易液化
【解析】解:(1)装置气密性的检查:连接好装置后,用弹簧夹夹住B构成封闭体系,向分液漏斗中加水并打开活塞,漏斗中的液面高度不变,说明气密性良好,故答案为:B;液面(水面)不下降;
故答案为:B; 液面高度不再变化;
(2)依据方程式MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,消耗4mol氯化氢生成1mol氯气,转移2mol电子,
MnCl2+Cl2↑+2H2O,消耗4mol氯化氢生成1mol氯气,转移2mol电子,
故答案为:2;
(3)实验过程中看到集气瓶中有黄绿色液滴,说明氯气具有的性质是易液化,
故答案为:易液化.
(1)根判断装置气密性的操作方法进行回答;
(2)依据方程式计算转移电子数;
(3)氯气沸点高,易液化.


科目:高中化学 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g100mL﹣1).
(1)实验步骤
①用(填仪器名称)量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL(填仪器名称)中定容,摇匀即得待测白醋溶液.
②用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴作指示剂.
③读取盛装0.100 0molL﹣1 NaOH 溶液的碱式滴定管的初始读数.如果液面位置如图所示,则此时的读数为mL.![]()
④滴定.当时,
停止滴定,并记录NaOH溶液的终读数.重复滴定3次.
(2)实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
数据处理与讨论
①按实验所得数据,可得c(市售白醋)=molL﹣1(列式计算);市售白醋总酸量=g100mL﹣1(列式计算).
②在本实验的滴定过程中,下列操作会使实验结果偏大的是填写序号).
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3molO2加入到VL的反应器中,在高温下放电,经t1s建立了平衡体系:3O22O3 , 此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
A.
B.
C.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C,A处充入等质量的X、Y两种气体,且X、Y的气体密度相等.当隔板停止滑动时,下列说法一定正确的是( )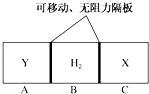
A.X、Y均为气体单质
B.物质的量:n(X)<n(H2)<n(Y)
C.X的相对分子质量等于Y的相对分子质量
D.隔板停止滑动时,A,B,C三部分体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)短周期元素R,T,Q,W在元素周期表中的相对位置如图所示,其中Q单质可制成半导体材料.下列判断正确的是( ) 
A.W形成的离子半径大于T形成的离子半径
B.W的单质在过量氧气中燃烧生成WO3
C.最高价氧化物的水化物的酸性:R<Q
D.T是地壳中含量最多的金属元素,其单质的化学性质较活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验中欲快速制得H2,以下最合适的方法是()
A. 纯锌与稀H2SO4 B. 纯锌和浓H2SO4
C. 纯锌与稀盐酸 D. 粗锌(含铜杂质)与稀H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学实验操作或事故处理方法错误的是
A. 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
B. 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸
C. 酒精灯着火时可用湿抹布盖灭
D. 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,关于溶液的稀释下列说法正确的是( )
A.pH=3的醋酸溶液稀释100倍,pH=5
B.pH=4的H2SO4溶液加水稀释100倍,溶液中由水电离产生的c(H+)=1×10﹣6 molL﹣1
C.将1L 0.1molL﹣1的Ba(OH)2溶液稀释为2L,pH=13
D.pH=8的NaOH溶液稀释100倍,其pH=6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,将0.4mol/L CH3COOH 溶液和 0.2mol/L NaOH 溶液各 100mL 混合后,pH=5,(设混合后溶液总体积为两溶液体积之和)
(1)混合溶液中离子浓度由大到小的顺序是
(2)①c(CH3COO﹣)+c(CH3COOH)= mol/L②c(CH3COO﹣)﹣c(CH3COOH)= mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com