
【题目】2SO2(g)+O2(g)![]() 2SO3(g) △H=-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO2+SO3(快); 4VO2+O2→2V2O5(慢),下列说法正确的是( )
2SO3(g) △H=-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO2+SO3(快); 4VO2+O2→2V2O5(慢),下列说法正确的是( )
A.反应速率主要取决于V2O5的质量B.VO2是该反应的催化剂
C.该反应逆反应的活化能大于198kJ/molD.升高温度,该反应的△H增大
【答案】C
【解析】
在V2O5存在时,该反应机理为:V2O5+SO2→2VO2+SO3(快); 4VO2+O2→2V2O5(慢),可知,V2O5是反应的催化剂,催化剂的催化效果与催化剂和反应物的接触面积有关,反应热等于正反应的活化能减去逆反应的活化能。
A. 由反应机理可得,V2O5是该反应的催化剂,反应速率与催化剂V2O5的质量有一定关系,但主要取决于催化剂V2O5的表面积,故A错误;
B. 反应中的催化剂是V2O5,而不是VO2,故B错误;
C. △H=正反应的活化能-逆反应的活化能=-198kJ/mol,所以逆反应的活化能大于198kJ/mol,故C正确;
D. 焓变与反应物、生成物的总能量的相对大小有关,而与外界条件无关,所以升高温度,该反应的△H不变,故D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.48g正丁烷和10g异丁烷的混合物中共价键数目为13NA
B.3.4g羟基(-OH) 和3.4g氢氧根(OH-)均含有2NA个电子
C.7.8g 苯含有碳碳双键的数目为0.3NA
D.标准状况下,22.4L 由CHCl3和CH2Cl2组成的混合物中含有的分子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断正确的是( )
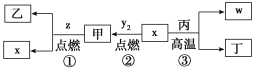
A.反应①、②属于氧化还原反应,③属于非氧化还原反应
B.Y的离子半径比Z的离子半径小
C.反应③可以证明X的非金属性强于W
D.一定条件下,x与甲反应生成丁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有0.1mol·L-1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是( )
①电离程度增大②[NH3·H2O]增大③![]() 数目增多④[OH-]增大⑤导电性增强⑥
数目增多④[OH-]增大⑤导电性增强⑥![]() 增大⑦
增大⑦![]() 减小
减小
A.①②③B.①③⑤C.①③⑥D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法错误的是
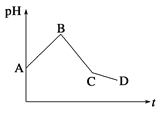
A.阳极先析出Cl2,后析出O2,阴极先产生Cu,后析出H2
B.AB段阳极只产生Cl2,阴极只产生Cu
C.BC段表示在阴极上是H+放电产生了H2
D.CD段相当于电解水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同温度下,三个体积均为1L的密闭容器中发生反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H=-867 kJ.mol-1,实验测得起始、平衡时的有关数据如表。下列说法正确的是
N2(g)+CO2(g)+2H2O(g) △H=-867 kJ.mol-1,实验测得起始、平衡时的有关数据如表。下列说法正确的是
容器编号 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | ||||
CH4 | NO2 | N2 | CO2 | H2O | NO2 | ||
I | T1 | 0.50 | 1.2 | 0 | 0 | 0 | 0.40 |
II | T2 | 0.30 | 0.80 | 0.20 | 0.20 | 0.40 | 0.60 |
III | T3 | 0.40 | 0.70 | 0.70 | 0.70 | 1.0 | |
A.T1<T2
B.若升高温度,正反应速率减小,逆反应速率增大,平衡逆移
C.平衡时,容器I中反应放出的热量为693.6 kJ
D.容器III中反应起始时v 正(CH4) <v逆(CH4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气脱硝脱碳的主要原理为2NO(g)+2CO(g)N2(g)+2CO2(g) ΔH<0。在一定温度下,体积固定为2L的密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如表所示:
时间/s | c(NO)/(mol·L-1) | c(CO)/(mol·L-1) |
0 | 9.50×10-3 | 9.00×10-3 |
1 | 4.50×10-3 | 4.00×10-3 |
2 | 2.50×10-3 | 2.00×10-3 |
3 | 1.50×10-3 | 1.00×10-3 |
4 | 1.50×10-3 | 1.00×10-3 |
下列说法正确的是
A.前2 s内的平均反应速率v(N2)=3.5×10-3mol·L-1·s-1
B.升高温度时,逆反应速率增大,正反应速率减小
C.容器内气体压强不再发生变化时,反应达到平衡状态
D.容器中气体的浓度c(NO):c(CO):c(N2):c(CO2)=2:2:1:2时,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.要证明硫酸亚铁铵晶体中含有![]() ,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体
,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体
B.![]() 、
、![]() 、
、![]() 等强氧化剂或其混合物不能研磨,否则将引起爆炸
等强氧化剂或其混合物不能研磨,否则将引起爆炸
C.常温下用pH试纸分别测定![]() 溶液和
溶液和![]() 溶液的pH,可以比较浓度对水解程度的影响
溶液的pH,可以比较浓度对水解程度的影响
D.过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应方程式不正确的是
A.氯气与水反应的离子方程式:Cl2+H2O![]() HClO+H++Cl-
HClO+H++Cl-
B.制备硝基苯的化学方程式:![]() +HO-NO2
+HO-NO2![]()
![]() NO2+H2O
NO2+H2O
C.碳酸钾水解的离子方程式:CO32-+2H2O=H2CO3+2OH-
D.钠与水反应的离子方程式:2Na+2H2O=2Na++2OH-+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com