
【题目】亚铁氰化钾的化学式为K4Fe(CN)6,一种用含NaCN废水合成该化合物的主要工艺流程如下:
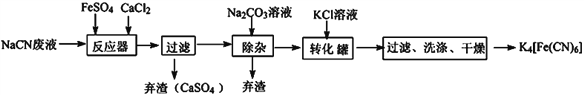
(1)请依据工艺流程图中的信息,回答下列问题:
①在“除杂”步骤中弃渣的主要成分为__________________(填化学式)。
②在“反应器“中发生的主要反应的化学方程式为:________________________________;
③相同温度下溶解度:Na4[Fe(CN)6]________K4[Fe(CN)6] (选填“>”、“<”或“=”)
(2)氰化钠(NaCN)是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。NaCN 的电子式为__________________________;实验室用NaCN固体配制NaCN溶液时,应先将其溶于氢氧化钠溶液中,再用蒸馏水稀释。NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是______________________________________。
(3)已知:氢氰酸是一种有苦杏仁气味的无色剧毒液体,易挥发,25℃时,Ka(HCN)=6.25×10-10。
①处理含CN-废水的方法是:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5-8.5,用NaClO完全氧化OCN-生成N2和两种盐。
请写出第二步反应的离子方程式:_________________________________________。
②反应CN-+H2O![]() HCN+OH-在25℃时的平衡常数K=_____________(填数值)。
HCN+OH-在25℃时的平衡常数K=_____________(填数值)。
(4)K4Fe(CN)6与高锰酸钾溶液反应,其方程式为:
K4Fe(CN)6+KMnO4 +H2SO4=KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平), 若有1mol K4Fe(CN)6被高锰酸钾氧化时,则消耗KMnO4的物质的量为________mol。
【答案】 CaCO3 6NaCN+FeSO4+ CaCl2=CaSO4↓+Na4Fe(CN )6+2NaCl > ![]() CN-+H2O2+ H2O= HCO3-+ NH3↑ 2CNO-+3C1O-+2H2O=N2+3Cl-+2HCO3- 1.6×10-5 12.2
CN-+H2O2+ H2O= HCO3-+ NH3↑ 2CNO-+3C1O-+2H2O=N2+3Cl-+2HCO3- 1.6×10-5 12.2
【解析】试题分析:由流程可知,在反应器中发生反应6NaCN+FeSO4+ CaCl2=CaSO4↓+Na4Fe(CN )6+2NaCl,过滤后除去硫酸钙,向滤液中加入碳酸钠溶液,把溶液中的钙离子转化为碳酸钙除去,再向滤液中加入氯化钾溶液与Na4Fe(CN )6发生复分解反应生成溶解度更小的K4Fe(CN )6,过滤、洗涤、干燥得到K4Fe(CN )6。
(1)①在“除杂”步骤中弃渣的主要成分为CaCO3。②在“反应器“中发生的主要反应的化学方程式为6NaCN+FeSO4+ CaCl2=CaSO4↓+Na4Fe(CN )6+2NaCl;③相同温度下溶解度:Na4[Fe(CN)6] >K4[Fe(CN)6] 。
(2)NaCN 的电子式为![]() ; NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,则该酸式盐为碳酸氢钠,该气体为氨气,该反应的离子方程式是CN-+H2O2+ H2O= HCO3-+ NH3↑。
; NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,则该酸式盐为碳酸氢钠,该气体为氨气,该反应的离子方程式是CN-+H2O2+ H2O= HCO3-+ NH3↑。
(3)①处理含CN-废水的方法是:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5-8.5,用NaClO完全氧化OCN-生成N2和两种盐,由组成元素可知,这两种盐为氯化钠和碳酸氢钠,第二步反应的离子方程式为2CNO-+3C1O-+2H2O=N2+3Cl-+2HCO3-。②反应CN-+H2O![]() HCN+OH-,在25℃时该反应的水解平衡常数K=
HCN+OH-,在25℃时该反应的水解平衡常数K=![]() 1.6×10-5。
1.6×10-5。
(4)K4Fe(CN)6与高锰酸钾溶液反应,其方程式为K4Fe(CN)6+KMnO4 +H2SO4=KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平),该反应中,K4Fe(CN)6中的Fe、C、N的化合价分别由+2、+2、-3升高到+3、+4、+5,KMnO4 中的Mn的化合价由+7下降到+2,根据化合价升降的总数相等,得到关系式10K4Fe(CN)6~122KMnO4, 所以,1mol K4Fe(CN)6被高锰酸钾氧化时,消耗KMnO4的物质的量为12.2mol。


科目:高中化学 来源: 题型:
【题目】用18 mol·L-1 浓硫酸配制90 mL 3.0 mol·L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积
②量取一定体积的浓硫酸
③溶解
④
⑤转移、洗涤
⑥定容、摇匀
⑦装瓶贴标签
完成下列问题:
(1)所需浓硫酸的体积是_____________,量取浓硫酸所用的量筒的规格是 _____________(从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。浓硫酸稀释的操作______________。
(2)第④步实验的操作是_______________________________________________________
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.用量筒量取浓硫酸后洗涤量筒并将洗涤液注入容量瓶内___________________;
B.容量瓶用蒸馏水洗涤后残留有少量的水________________;
C.所用过的烧杯、玻璃棒未洗涤________________;
D.定容时俯视刻度线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配置100 mL 1.0×10-2 mol·L-1的CuSO4溶液,下列玻璃仪器中,一定要用到的有( )
A. 漏斗 B. 玻璃棒 C. 烧杯 D. 容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,下列操作或发生事故时的处理方法正确的是
A. 可用燃着的酒精灯引燃另一只酒精灯。
B. 给试管里的液体加热时,试管应与桌面垂直。
C. 配置一定浓度的NaCl溶液时,定容振荡摇匀后,发现液面低于刻度线,再加水到刻度线。
D. 浓硫酸不慎沾在皮肤上,应立即用大量水冲洗,最后涂上3%-5%的小苏打溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 1 mol氩气在标准状况下的体积约为11.2 L
B. 20 ℃、10 MPa状态下,32 g O2和O3的混合气体所含原子数为2.5NA
C. 标准状况下,11.2 L H2CO3含有的原子数为3NA
D. 常温常压下,44 g CO2含有的原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月18日,中国国土资源部地质调查局宣布,我国在南海进行的可燃冰试采获得成功,成为全球第一个海域试采可燃冰成功的国家,可燃冰即天然气水合物,甲烷含量占80%至99.9%。化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇或合成氨,回答下列问题:
(1)甲醇是一种用途广泛的化工原料,工业上常用下列两种反应制备甲醇:
CO(g)+2H2(g)=CH3OH(g) △H1 =-90kJ·mol-1 K1
CO2(g)+3H2(g)= CH3OH(g)+H2O(l) △H2 K2
己知: CO(g)+H2O(g)= CO2(g)+H2(g) △H3 =-41.1kJ·mol-1 K3
H2O(l)=H2O(g) △H4 =+44.0kJ·mol-1 K4
则K2=_______ (用含K1、K3、K4的代数式表示)
(2)在一恒温恒容密闭容器中充入1molCO2和3molH2模拟工业合成甲醇的反应:CO2(g)十3H2(g) ![]() CH3OH(g)十H2O(g)
CH3OH(g)十H2O(g)
①下列能说明该反应已达到平衡状态的是______________________。
A.混合气体平均相对分子质量不变 B.混合气体密度不变
C.容器内压强恒定不变 D.反应速率满足以下关系:V正(CO2)=3V逆(H2)
E.CO2、H2、CH3OH、H2O物质的量浓度之比为1:3:1:1
F.单位时间内断裂3NAH-H键的同时形成2molH-O键
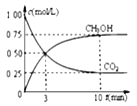
②模拟过程中测得CO2和CH3OH(g)浓度随时间变化如图所示,若此时容器内压强为P,则用平衡分压代替平衡浓度表示的化学平衡常数KP为_____________(用含P的代数式表示,数值保留两位小数),若此时再向容器内充入0.25molCO2和0.25molCH3OH的混合气体,则平衡______(填“正向“逆向“不”)移动。(已知:气体分压=气体总压×体积分数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“化学是你,化学是我”.化学与生产、生活密切相关,下列说法错误的是( )
A. 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
B. 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质
C. 开发利用太阳能、风能、生物能、海洋能等清洁能源,符合“低碳经济”
D. 二氧化硫有漂白性,常用于棉、麻、纸张和食品的漂白
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下列各图所示是中学化学中常用于混合物分离和提纯的装置:
A. 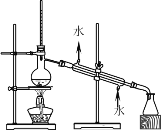 B.
B. 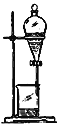
C.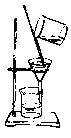 D.
D. 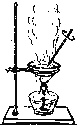
请根据装置图回答下列问题:
⑴A图中用于盛放液体混合物的仪器的名称为:__________________
⑵选择合适的实验装置分离以下混合物(填代表装置的字母),
①从碘水中分离出I2 : ___________
②进行酒精和水的分离: ___________
③二氧化锰和蔗糖溶液: ___________
⑶我国具有历史悠久的酒文化,请回答下列问题:
①要提高酒精的度数,可采用的方法是________________(填操作方法,下同)
②中药常常浸泡在美酒中制成药酒,你认为利用的方法是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com