
����Ŀ���ɽ���߷��Ӳ���P�ĽṹΪ�� ����ͼ��P�ĺϳ�·�ߡ�
����ͼ��P�ĺϳ�·�ߡ�

��֪��![]() +R3OH
+R3OH![]() +R2OH
+R2OH
��1��B�Ľṹ��ʽ��_______���Լ�a��_______��
��2��![]() �й����ŵ�������_____��_____��
�й����ŵ�������_____��_____��
��3���۵Ļ�ѧ����ʽ��______��
��4���ķ�Ӧ������_____��
��5��G��E��Ϊͬ���칹�壬��������Ҫ���G����______�֡�(�����������칹)
�ٺ��к�E(C6H10O3)��ͬ�ĺ��������Ţڷ����к�����Ԫ��״�����ṹ
��6�������з�Ӧ�������ʵ���֮��1��1������Ӧʱ����Ӧ�ݵĻ�ѧ����ʽ��_____��
���𰸡�BrCH2CH2Br NaOHˮ��Һ ̼̼˫�� �Ȼ� ![]() ȡ����Ӧ 20
ȡ����Ӧ 20 ![]()
��������
�ɺϳ����̿�֪��AΪCH2=CH2��A�����ӳɷ�Ӧ����BΪBrCH2CH2Br��B����ˮ�ⷴӦ����DΪHOCH2CH2OH��D��2-����ϩ�ᷢ��������Ӧ����E����E�Ľṹ��ʽΪ![]() �����з�����Ϣ�еĽ�����Ӧ����FΪ
�����з�����Ϣ�еĽ�����Ӧ����FΪ![]() ��F�������۷�Ӧ����
��F�������۷�Ӧ����![]() ����Ϊȡ����Ӧ�����ϳɸ߷���P���Դ������
����Ϊȡ����Ӧ�����ϳɸ߷���P���Դ������
(1)�ɷ���֪��B�Ľṹ��ʽ��BrCH2CH2Br����Ӧ��Ϊ±������ˮ�ⷴӦ�����Լ�a��NaOHˮ��Һ��
(2)![]() �еĹ�������̼̼˫�����Ȼ���
�еĹ�������̼̼˫�����Ȼ���
(3)��Ӧ��Ϊ������Ӧ����Ӧ�Ļ�ѧ����ʽ��![]() ��
��
(4)�ķ�Ӧ������ȡ����Ӧ��
(5)G��E��Ϊͬ���칹�壬�Һ�����ͬ�ĺ��������ż��Դ��������ʹ��ǻ���������ӽṹ�к�����Ԫ��״�����ṹ�� ������һ��-CH2OH��һ��-CH3��-OH������Ԫ��״��������һ��-CH2OH����4�֣���Ԫ��״��������-CH3��-OH������-CH3��-OH�ֱ�������������ͬ��̼ԭ���Ϲ���12�֣�������ͬһ��̼ԭ���Ϲ���4�֣������Ҫ���G����20�ֽṹ��
������һ��-CH2OH��һ��-CH3��-OH������Ԫ��״��������һ��-CH2OH����4�֣���Ԫ��״��������-CH3��-OH������-CH3��-OH�ֱ�������������ͬ��̼ԭ���Ϲ���12�֣�������ͬһ��̼ԭ���Ϲ���4�֣������Ҫ���G����20�ֽṹ��
(6)�����з�Ӧ�������ʵ���֮��1��1������Ӧʱ����Ӧ�ݵĻ�ѧ����ʽ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������Ҵ���Ũ���ᷴӦ�Ʊ���ϩ����ѧ����ʽΪ��C2H5OH![]() CH2=CH2��+H2O����������Һ������ϩ��Ӧ�Ʊ�1��2-�������顣���Ʊ����������ڲ����Ҵ���Ũ���ᷢ��������ԭ��Ӧ�������CO2��SO2,��������Br2��Ӧ����HBr���������塣ijѧϰС������������Ϊԭ�ϣ���װ�����������̽ӿڻ���Ƥ�ܾ�����ȥ�����Ʊ�1,2-��������
CH2=CH2��+H2O����������Һ������ϩ��Ӧ�Ʊ�1��2-�������顣���Ʊ����������ڲ����Ҵ���Ũ���ᷢ��������ԭ��Ӧ�������CO2��SO2,��������Br2��Ӧ����HBr���������塣ijѧϰС������������Ϊԭ�ϣ���װ�����������̽ӿڻ���Ƥ�ܾ�����ȥ�����Ʊ�1,2-��������
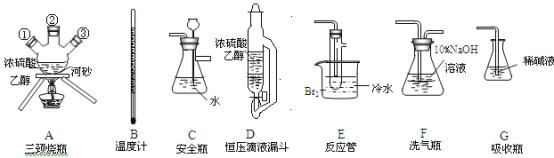
��1�����������������ң���ȷ������˳���ǣ�
B��A������A��D��������A����__��__��___��___��
��2���¶ȼ�ˮ�������ȷλ����_________��
��3��װ��D�����©����ȣ�����Ҫ�ŵ���_______��
��4��װ��C����Ҫ������_______��װ��F��������__________��
��5���ڷ�Ӧ��E�н��е���Ҫ��Ӧ�Ļ�ѧ����ʽΪ________��
��6��װ��E�ձ��е���ˮ�ͷ�Ӧ����Һ���ϵ�ˮ�����þ���_______________������װ��F�������E�е���Ҫ��ӦΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�¶���CH3COOH��NH3��H2O�ĵ��볣�����,����10 mLŨ��Ϊ0.1 mol/L��CH3COOH��Һ�еμ���ͬŨ�ȵİ�ˮ,�ڵμӹ�����(����)
A. �����백ˮ�����Ϊ10 mLʱ,c(NH4+)=c(CH3COO-)
B. c(NH4+)/c(NH3��H2O)�������ټ�С
C. ˮ�ĵ���̶�ʼ������
D. c(CH3COOH)��c(CH3COO-)֮��ʼ�ձ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2H2��O2![]() 2H2O��
2H2O��
��1���÷�Ӧ1g������ȫȼ�շų�����121.6kJ�����ж���1molH-H������436kJ������1molO=O������496kJ����ô�γ�1molH-O���ų�����____________________��
��2��ԭ�����ֱ�Ӱѻ�ѧ��ת��Ϊ���ܵ�װ�á�
I.���켼����ʹ�õ��⣭��ȼ�ϵ�ؾ��и��ܡ����Ͳ���Ⱦ�������ŵ㡣��ͼ���⣭��ȼ�ϵ�ص�װ��ͼ����

����Һ��OH-����________�缫������a������b������
��b�缫����pH_____________��(������С��)
�����H2��Ϊ��������缫��ӦʽΪ��������____________________________��������________________________________��
II.��пƬ����Ƭ����ϡ���������ԭ��أ����缫������һ�������������õ�������缫��������Ϊ60g������һ��ʱ���ȡ��пƬ����Ƭϴ���������أ�������Ϊ47g���Լ��㣺�������������___________________________________L������״����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA Ϊ�����ӵ�������ֵ������˵����ȷ���� ( )
A.18g![]() ��
��![]() �Ļ�����У�����������Ϊ 10 NA
�Ļ�����У�����������Ϊ 10 NA
B.��״���£�2.24L SO3 �к��е���ԭ����ĿΪ 0.3 NA
C.���ʵ���Ũ��Ϊ 0.1molL��1 �� MgCl2 ��Һ�У����� Cl������Ϊ 0.2 NA
D.һ�������£�2.3g �Ľ�������ȫ��������Ӧʱ���� 3.6g ����ʱʧȥ�ĵ�����Ϊ 0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲ���ԲͲ��ʢ��������ɫ�Ļ������ܵ�����Һ�塣�ϲ�Һ���в�������ʯī�缫��ԲͲ�ڻ�����һ���¶���ɻ�״�IJ����������������½���Һ�壬װ������ͼ����ͨ��Դ��������Χ��Һ�������ɫ������ɫ��dz������������������ɡ�ֹͣͨ�磬ȡ���缫���ý������¾��ҽ��������ú�Һ���ֳַ����㣬�²�Һ����Ϻ�ɫ���ϲ�Һ�弸����ɫ�������ж�����ȷ����(����)

A. ԭ�ϲ�Һ�������KI��ˮ��Һ��ԭ�²�Һ�������CCl4
B. ���������Һ����ɫ�����仯��ԭ����I2��CCl4�е��ܽ�ȴ�����ˮ���ܽ�ȣ����Ծ���I2��ת�Ƶ�CCl4��
C. ��������pH�����ԭ����ˮ���ӵõ���������OH��
D. �����ϵĵ缫��Ӧʽ2H++2e - =H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������з������·�Ӧ��mA(g)+nB(g)![]() pC(g)���ﵽƽ������¶Ȳ��䣬�����������С��ԭ����һ�룬���ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ��1��9��������˵���������
pC(g)���ﵽƽ������¶Ȳ��䣬�����������С��ԭ����һ�룬���ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ��1��9��������˵���������
A. ƽ�����淴Ӧ�����ƶ�B. A��ת���ʽ���
C. m+n��pD. C�����������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦN2(g)+3H2(g)![]() 2NH3(g)��һ���ȷ�Ӧ�������Ӧ���ܱ������н��У������й�˵��������ȷ���ǣ� ��
2NH3(g)��һ���ȷ�Ӧ�������Ӧ���ܱ������н��У������й�˵��������ȷ���ǣ� ��
A. �����¶Ȼ�ʹ��Ӧ���ʼӿ�
B. ��NH3��Ũ�Ȳ��ٱ仯ʱ����Ӧ�ﵽ��ƽ��״̬
C. �ڸ��ºʹ��������£�H2����100%��ת��ΪNH3
D. ʹ�ô������Լӿ췴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ƽ�ⳣ������Ka��ʾ)�Ĵ�С�����жϵ���ʵ����ǿ����25��ʱ���й����ʵĵ���ƽ�ⳣ�����±���ʾ�����ݸñ����ش��������⣺
��ѧʽ | HF | CH3COOH | H2SO3 | H2CO3 | H2S |
����ƽ�� ������Ka�� | 7.2��10-4 | 1.8��10-5 | K1=1.54��10-2 K2=1.02��10-7 | K1=4.4��10-7 K2=4.7��10-11 | K1��9.1��10��8 K2��1.1��10��12 |
��1��ͬŨ�ȵ�F����CO32-��CH3COO-��HS-���H����������ǿ��Ϊ__________
��2����Һ�в����ܴ����������������__________
a��HS-��SO32- b��HF��CH3COO- c��HS-��HCO3- d. HSO3-��HCO3-
��3��Na2CO3��Һͨ�����H2S�����ӷ���ʽ�ǣ�___________��
��4����֪pH= -lgc��H+�������Ϊ10 mL pH��2�Ĵ�����Һ��һԪ��HX�ֱ��ˮϡ����1000 mL��ϡ������pH�仯��ͼ��ʾ����HX�ĵ���ƽ�ⳣ��______����ĵ���ƽ�ⳣ��(�>������<������)�� ����дһ�ַ���֤���������������________________��

��5���� 0.l molL-1 HF ��Һ�еμ� NaOH ��Һ��c(HF) : c(F-) =5 : 36����ʱ��ҺpH = _____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com