
实验室制备1,2-二溴乙烷的反应原理如下:
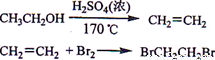
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
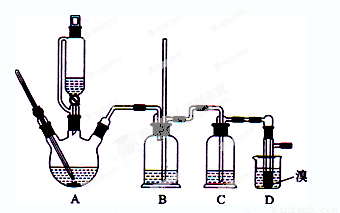
有关数据列表如下:
|
|
乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
状态 |
无色液体 |
无色液体 |
无色液体 |
|
密度/g · cm-3 |
0.79 |
2.2 |
0.71 |
|
沸点/℃ |
78.5 |
132 |
34.6 |
|
熔点/℃ |
一l30 |
9 |
-1l6 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是 ;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用 洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用 的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 。
(1)d (2)c (3)溴的颜色完全褪去 (4)下 (5)b (6)蒸馏
(7)避免溴大量挥发; 产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管
【解析】
试题分析:(1)因“乙醇在浓硫酸的存在下在l40℃易脱水生成乙醚”,故迅速地把反应温度提高到170℃左右的原因是减少副产物乙醚生成,答案选d。
(2) 浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应。因此根据装置C的“目的是吸收反应中可能生成的酸性气体”可知,在装置C中应加入氢氧化钠溶液,答案选c。
(3)是用“少量的溴和足量的乙醇制备1,2—二溴乙烷”,反应结束时溴已经完全被消耗,而1,2—二溴乙烷是无色的,所以断该制备反应已经结束的最简单方法是溴的颜色褪尽。
(4)由表中数据可知,1,2-二溴乙烷的密度大于水,因而在下层。
(5) Br2能与氢氧化钠溶液反应,故可用氢氧化钠溶液洗涤;虽然也能与碘化钠溶液反应,但生成的I2也溶于1,2-二溴乙烷,因此答案选b。
(6)根据表中数据,1,2-二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离 (不能用蒸发,乙醚不能散发到空气中)。
(7) 溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发。但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却,否则会使产品凝固而堵塞导管。
考点:考查溴乙烷制备的实验探究
点评:该题是高考中的常见题型,属于中等难度的试题。主要考查了乙醇制备1,2-二溴乙烷,涉及物质的分离与提纯,反应条件的控制等,有利于培养学生的逻辑推理能力和规范、严谨的实验设计能力。掌握相关物质的基本性质,是解答本题的关键,平时须注意知识的积累和总结,并能灵活运用即可。


科目:高中化学 来源: 题型:阅读理解
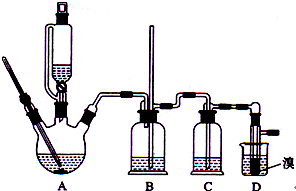 (2012?海南)实验室制备1,2-二溴乙烷的反应原理如下:
(2012?海南)实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g?cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g?cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 浓硫酸 |
| 170摄氏度 |
| 加热 |
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g?cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
| 加热 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
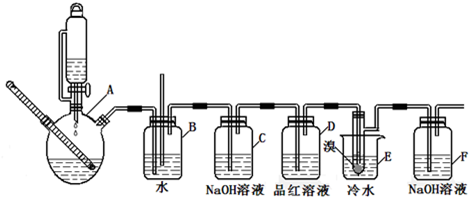
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省甘谷县甘谷一中高二下学期期中考试化学试卷(带解析) 题型:实验题
已知实验室制备1,2-二溴乙烷可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示: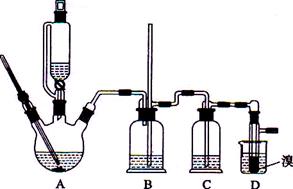
有关数据列表如下:
| | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com