
将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH
![]() 溶液。请回答:
溶液。请回答:
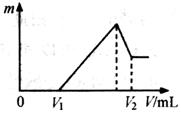
![]() ⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。当
⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。当
![]() V1=160mL时,则金属粉末中n(Mg)= mol,V2=
V1=160mL时,则金属粉末中n(Mg)= mol,V2=
![]() mL。
mL。
![]() ⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶 液的体积V(NaOH) mL。
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶 液的体积V(NaOH) mL。
![]() ⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是: 。
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是: 。
⑴0.06 mol,440 mL。⑵400 mL。 ⑶![]() ≤a<1。
≤a<1。![]()
![]()
![]()
![]()
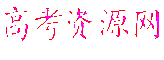
⑴由图像可知:V1 mL的NaOH溶液是与过量H2SO4反应的,则与Mg、
![]() Al反应的为H2SO4:0.2mol-0.16mol×=0.12mol。
Al反应的为H2SO4:0.2mol-0.16mol×=0.12mol。
![]() 假设n(Mg)=x mol,n(Al)=y mol,
假设n(Mg)=x mol,n(Al)=y mol,
![]() 则有方程组: 解得:
则有方程组: 解得:
![]() 当加入V2 mL NaOH溶液时,得到Mg(OH)2↓和NaAlO2,关系式为:
当加入V2 mL NaOH溶液时,得到Mg(OH)2↓和NaAlO2,关系式为:
![]() Mg2+~2OH-,Al3+~4OH-,
Mg2+~2OH-,Al3+~4OH-,
![]() 得:V2=160 mL+
得:V2=160 mL+![]() =440 mL。
=440 mL。
![]() ⑵当Mg2+、Al3+刚好沉淀完全时,溶液中只有Na2SO4,
⑵当Mg2+、Al3+刚好沉淀完全时,溶液中只有Na2SO4,
![]() 关系式为2NaOH~H2SO4,得:V(NaOH)=
关系式为2NaOH~H2SO4,得:V(NaOH)=![]() =400 mL。
=400 mL。
![]() ⑶当所得沉淀中无Al(OH)3时,NaOH溶液过量,反应后生成的溶质为:Na2SO4、NaAlO2。则根据Na元素守恒有:
⑶当所得沉淀中无Al(OH)3时,NaOH溶液过量,反应后生成的溶质为:Na2SO4、NaAlO2。则根据Na元素守恒有:
![]() n(NaOH)=0.45 L×1mol/L≥0.1 L×2 mol/L×2+0.1×(1-a)mol。
n(NaOH)=0.45 L×1mol/L≥0.1 L×2 mol/L×2+0.1×(1-a)mol。
![]() 解得a≥
解得a≥![]() ,则满足此条件的a的取值范围是
,则满足此条件的a的取值范围是![]() ≤a<1。
≤a<1。


科目:高中化学 来源: 题型:
将0.1 mol的镁、铝混合物溶于100mL 2mol·L![]() 的H2SO4溶液中,然后再滴加1mol·L
的H2SO4溶液中,然后再滴加1mol·L![]() 的NaOH溶液。请回答:(不需要写出计算过程)
的NaOH溶液。请回答:(不需要写出计算过程)
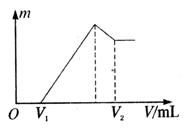
(1)若在滴加NaOH溶液的过程中沉淀质量![]() 随加入NaOH溶液的体积V变化如图所示。当
随加入NaOH溶液的体积V变化如图所示。当![]() mL时,则金属粉末中
mL时,则金属粉末中![]() (Mg)= mol,
(Mg)= mol,![]() mL。
mL。
(2)①要配制100 mL 2mol·L![]() 的H2SO4溶液,需要的仪器除量筒、烧杯外,还有 。
的H2SO4溶液,需要的仪器除量筒、烧杯外,还有 。
②下列操作会使所配的溶液浓度偏小的是( )(填代号)
A.用量筒量取一定体积的98%的浓H2SO4,稀释后未经冷却即转入容量瓶内
B.稀释硫酸所用的小烧杯未洗涤
C.定容时俯视液面
D.用蒸馏水洗涤后的容量瓶未干燥
E.定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液浅出瓶外
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.1 mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液至过量。请回答:
(1)写出与铝有关的离子方程式:
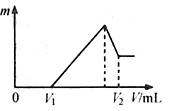
(2)若在滴加NaOH溶液过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)= mol,
V2= mL。沉淀的最大质量是 g。
(3)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)= mL。
(4)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是: 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年广东省高三上学期10月份月考(理综)化学卷 题型:填空题
将0.1 mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液至过量。请回答:

(1)写出与铝有关的离子方程式:
(2)若在滴加NaOH溶液过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)= mol,
V2= mL。沉淀的最大质量是 g。
(3)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)= mL。
(4)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是: 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山东省高三上学期期中考试化学试卷 题型:填空题
将0.1 mol的镁、铝混合物溶于100mL 2mol·L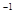 的H2SO4溶液中,然后再滴加1mol·L
的H2SO4溶液中,然后再滴加1mol·L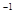 的NaOH溶液。请回答:(不需要写出计算过程)
的NaOH溶液。请回答:(不需要写出计算过程)

(1)若在滴加NaOH溶液的过程中沉淀质量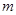 随加入NaOH溶液的体积V变化如图所示。当
随加入NaOH溶液的体积V变化如图所示。当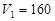 mL时,则金属粉末中
mL时,则金属粉末中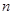 (Mg)= mol,
(Mg)= mol,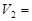 mL。
mL。
(2)①要配制100 mL 2mol·L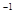 的H2SO4溶液,需要的仪器除量筒、烧杯外,还有 。
的H2SO4溶液,需要的仪器除量筒、烧杯外,还有 。
②下列操作会使所配的溶液浓度偏小的是( )(填代号)
A.用量筒量取一定体积的98%的浓H2SO4,稀释后未经冷却即转入容量瓶内
B.稀释硫酸所用的小烧杯未洗涤
C.定容时俯视液面
D.用蒸馏水洗涤后的容量瓶未干燥
E.定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液浅出瓶外
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com