
| A.1 mol羟基中含有10 NA个电子 |
| B.标准状况下,2.24 L苯中含有0.6NA个碳原子 |
| C.常温常压下,46g NO2和N2O4混合气体中含有的原子总数为3NA |
| D.1 mol Fe和稀稀硝酸反应生成NO气体,转移2NA个电子 |
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,22.4 L H2O中含有的分子数为NA |
| B.28 g N2中含有的分子数为NA |
| C.1 mol Mg与足量稀盐酸反应转移的电子数为NA |
| D.1 L 1 mol·L-1 Na2 CO3溶液中含有的钠离子数为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2O和Na2O2的混合物共1mol,阴离子数目在NA~2NA之间 |
| B.常温常压下,92 g NO2和N2O4的混合气体中含有的分子数目为2NA |
| C.一定条件下,密闭容器充入1molN2和3molH2充分反应,转移电子的数目为6NA |
| D.FeCl3溶液中,若Fe3+数目为NA,则Cl—数目大于3NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.9.2 g C7H8和C3H8O3的混合物中所含氢原子总数为0.8 NA |
| B.标准状况下,11.2 L C2H5OH中所含的分子数为0.5 NA |
| C.将含0.1 mol FeCl3的溶液滴加到沸水中完全水解可生成0.1 NA个Fe(OH)3胶粒 |
| D.0.1 mol Na2O2参加反应转移的电子数目是0.2 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应过程中得到3.36L(标准状况)的气体 |
| B.反应结束得到3.9g的沉淀 |
| C.反应结束得到的溶液中c(Na+)= c(Cl-)+ c(OH-) |
| D.反应结束得到的溶液中c(NaCl)="1.0" mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
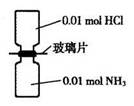
| A.气体反应物的总体积为0.448L |
| B.装置中氢元素的总质量为0.04g |
| C.生成物中含有0.01NA个分子 |
| D.生成物完全溶于永后所得溶液含有0.01 NA个NH4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编 号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 mL | 200 mL | 300 mL | 400 mL |
| 剩余金属/g | 18.0 g | 9.6 g | 0 | 0 |
| NO体积/L | 2.24 L | 4.48 L | 6.72 L | V |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 molCH4分子中共价键总数为NA |
| B.水的摩尔质量就是NA个水分子的质量之和 |
| C.含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| D.1 mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com