
【题目】反应A(g)+2B(g)![]() C(g)+D(g) △H=-QkJ·mol-1的能量变化如图所示,有关叙述正确的是( )
C(g)+D(g) △H=-QkJ·mol-1的能量变化如图所示,有关叙述正确的是( )
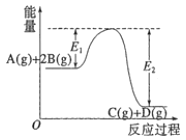
A.Q=E1-E2
B.在反应体系中加入催化剂,反应速率增大,E1减小,E2不变
C.Q>0,升高温度,正反应速率增大,逆反应速率减小
D.若减小体积,平衡会移动,当反应再次达到平衡时,A的平衡浓度增大
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】海洋中有丰富的资源,下图为海水资源利用的部分过程。
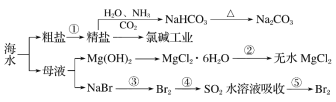
下列有关说法正确的是( )
A.用澄清石灰水可鉴别NaHCO3和Na2CO3
B.第③步和第⑤步均发生了氧化还原反应
C.在第③④⑤步中溴元素均被氧化
D.将MgCl2·6H2O加热蒸发可得无水MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为0.1mol·L-1的下列溶液:①盐酸 ②醋酸 ③氢氧化钠 ④氯化铵 ⑤硫酸氢铵 ⑥氨水,请回答下列问题:
(1)已知t ℃时,Kw=1×10-13,则t ℃(填“>” “<”或“=”)__25℃。
(2)②③④三种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)____。
(3)已知④溶液呈酸性,请用离子方程式表示___。
(4)④⑤⑥四种溶液中NH4+浓度由大到小的顺序是(填序号)____。
(5)常温下,将①和③按体积比2:1混合后,溶液的pH约为____(已知lg3=0.5)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确的是 ( )

A.电负性:![]()
B.离子半径:![]()
C.![]() 分子中各原子的最外层均满足8电子稳定结构
分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子的最外层电子排布图为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①2CO(g)+O2(g)![]() 2CO2(g) ΔH=566.0kJ/mol
2CO2(g) ΔH=566.0kJ/mol
②N2(g)+O2(g)![]() 2NO(g) ΔH=+180.5kJ/mol
2NO(g) ΔH=+180.5kJ/mol
③2NO(g)+O2(g)![]() 2NO2(g) ΔH=116.5kJ/mol
2NO2(g) ΔH=116.5kJ/mol
回答下列问题:
(1)CO的燃烧热为___。若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为___kJ。
(2)CO将NO2还原为单质的热化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y是主族元素,I为电离能,单位是![]() 。请根据下表所列数据判断下列说法,其中错误的是
。请根据下表所列数据判断下列说法,其中错误的是![]()
![]()
元素 |
|
|
|
|
X | 500 | 4600 | 6900 | 9500 |
Y | 580 | 1800 | 2700 | 11600 |
A.元素X常见化合价是![]()
B.元素Y是第ⅢA族元素
C.同周期主族元素中,X的第一电离能最小
D.若元素Y处于第三周期,它可与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的分子式为![]() ,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为
,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为![]() 和
和![]() ,下列推断不正确的是
,下列推断不正确的是
A.![]() 分子的空间构型为“V”形
分子的空间构型为“V”形
B.![]() 键为极性共价键,
键为极性共价键,![]() 分子为非极性分子
分子为非极性分子
C.![]() 与
与![]() 相比,
相比,![]() 的熔点、沸点比
的熔点、沸点比![]() 的低
的低
D.![]() 分子的中心原子的成键轨道为
分子的中心原子的成键轨道为![]() 杂化轨道
杂化轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙腈主要用于有机合成及生产医药,农药的中间体,对环境有危害。常温常压下,苯乙腈水解一般需加入酸碱催化剂。但研究人员发现,在近临界水(指温度在523~623K之间的压缩液态水)中,不加任何催化剂的情况下,苯乙腈就能发生水解反应生成苯乙酞胺:
C6H5CH2CN(l)+H2O(l) ![]() C6H5CH2CONH2(l) △H
C6H5CH2CONH2(l) △H
(苯乙腈) (苯乙酰胺)
请回答下列问题:
(1)已知近临界水中,水的离子积常数为10-10,则此条件下,pH=7的NaAc溶液中由水电离的c(H+)=________ mol·L-1。该反应不加任何催化剂就能发生的主要原因是____________。
(2)研究反应的平衡常数(记作lgK)与温度(T)的关系,得到如图1所示的关系,判断该反应的△H__________0(填“>”“<”或“=”)。
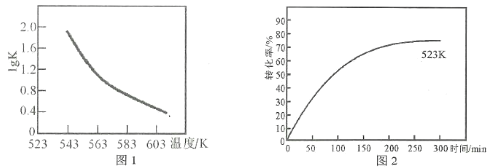
(3)图2表示其他条件不变时,温度和时间对苯乙腈转化率的影响曲线图(不完整)。若图中曲线对应的温度为523K,请你在原图中作出温度为583K的影响曲线。___________。
(4)下列仪器可用于测定苯乙腈相对分子质量的是_________(填编号)。
A.元素分析仪 B.核磁共振仪 C.红外光谱仪 D.质谱仪
(5)水的用途很广,可利用太阳能光伏电池电解水制高纯氢,工作示意图如图。通过控制开关连接K1或K2,可交替得到H2和O2。
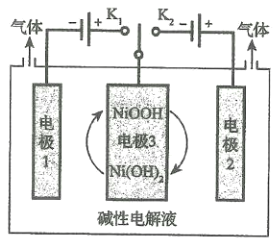
①制H2时,连接______________,可得H2。
②改变开关连接方式,产生O2的电极反应式__________________________。
③选用NiOOH、Ni(OH)2作为电极3材料的优点(请结合电极反应式进行阐述)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如下物质的转化关系图,回答有关问题:

(1)上述物质中,_________(填结构简式,下同)的产量是衡量一个国家石油化工发展水平的标志;常见的酸性调味品中含有3%~5%的_________;具有香味的油状液体是_____________。
(2)乙烯的工业制法是_________。
a.石油裂化 b.煤干馏 c.石油裂解 d.石油分馏
(3)乙醛中的官能团名称是______,比乙醛少一个碳原子的同系物的结构简式是______。
(4)工业上用乙烯水化法制乙醇,乙烯在加热、加压和催化剂存在的条件下,跟水反应生成乙醇,该反应的化学方程式是_______________________。
(5)生成乙酸乙酯的化学方程式是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com