
下列有关实验的叙述正确的是
| A.用水润湿的pH试纸来测量溶液的pH |
| B.实验室需要480 mL 2.0 mol·L-1的氢氧化钠溶液,配制该溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、移液、洗涤、定容、摇匀的步骤进行操作 |
| C.用溴水、淀粉-KI溶液比较Br2与I2的氧化性强弱,所需玻璃仪器主要有:试管、胶头滴管 |
| D.向溶液中滴加硝酸酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
科目:高中化学 来源: 题型:单选题
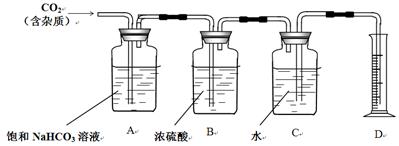
下列有关实验装置进行的相应实验,能达到实验目的的是
| A.图1定量测定H2O2的分解速率 |
| B.图2装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.图3装置测量Cu与浓硝酸反应产生气体的体积 |
| D.图4证明CH3CH2OH发生消去反应生成了乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验的叙述,正确的是
| A.用碱式滴定管量取20.00mL KMnO4溶液 |
| B.用玻璃棒蘸取浓硫酸点在pH试纸上,测其pH |
| C.取用一小块钠后,剩余的钠放到垃圾桶里 |
| D.配制一定物质的量浓度的稀硫酸时,定容时俯视,则所配溶液的浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验操作与实验目的或结论一致的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某溶质中先滴加稀硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| B | 将混合气通过饱和的Na2CO3溶液 | 除去CO2中混有的HCl |
| C | 配制SnCl2溶液时,先将SnCl2溶于适量的稀盐酸中,再用蒸馏水稀释,保存时在试剂瓶中加入少量的锡粒 | 抑制Sn2+水解,并防止Sn2+被氧化为Sn4+ |
| D | 将苯滴入溴水中,振荡,静置,溴水层褪色 | 溴或苯发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于实验原理或操作的叙述中,不正确的是
| A.判断皂化反应是否完全,可取反应后的混合液滴入热水中 |
| B.减压过滤不宜过滤胶状沉淀或颗粒太小的沉淀 |
| C.制备硫酸亚铁铵晶体,需加热至大量晶体析出并剩余少量液体即停止加热 |
| D.易燃试剂与强氧化性试剂需分开放置,并远离火源;金属着火时.可用细沙覆盖灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验的说法正确的是
| A.用pH试纸蘸取NaOH溶液,立刻与比色卡对比,测定NaOH溶液的Ph |
B.通过观察图中导管水柱的变化,验证铁钉生锈的原因主要是吸氧腐蚀 |
| C.均不能采取将溶液直接蒸干的方法制得AIC13、A12(SO4)3、FeC13、Fe2(SO4)3 |
| D.滴定用的滴定管、锥形瓶和配制一定物质的量浓度溶液用的容量瓶,使用前均要润洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于下列实验的叙述中正确的是
| A.溴乙烷在浓硫酸作用下加热可制得乙烯. |
| B.在制备乙酸乙酯实验中,长导管有冷凝蒸汽和导气的作用,饱和碳酸钠溶液液面上有油状并有香味液体生成 |
| C.实验室可用无水乙醇和过量的3mol/L硫酸的混合液制乙烯 |
| D.用电石和水可制得纯净的乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一。重庆一中某化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究。
I. 甲同学老家在山西,对儿时在家乡品尝到的山西老陈醋的滋味记忆犹新,跟随父母来到重庆后,总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知以下信息:
①醋分两种,酿造醋和配制醋。正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋。
②酿造醋国家标准为醋酸含量必须大于3.50 g/100mL,而配制醋国家标准仅为1.50 g~3.50g/100mL。
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L。
(1)请帮助张同学计算从超市购买的食醋中醋酸含量为_______g/100mL,属于____________醋(填“酿造”或“配制”)。(提示:醋酸摩尔质量为60g/mol)
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式_______________________________。
II. 下图是重庆一中化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配100mL1mol/L的稀盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
(1)配制稀盐酸时,还缺少的仪器有 ;
(2)经计算,配制100mL1mol/L的稀盐酸需要用量筒量取上述浓盐酸的体积为 mL(保留小数点后一位);
(3)对所配制的稀盐酸进行测定,发现其浓度小于1mol/L,引起误差的原因可能是 。
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶在使用前未干燥,里面有少量蒸馏水 |
| C.转移溶液后,未洗涤烧杯和玻璃棒 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com