
【题目】50mL0.50 mol·L-1盐酸与50mL0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
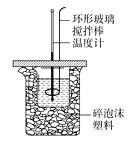
(1)大小烧杯间填满碎泡沫塑料的作用是_____。
(2)大烧杯上如不盖硬纸板,求得的中和热数值将____(填“偏大”“偏小”或“无影响”)。
(3)实验中改用60mL0.50 mol·L-1盐酸与50mL0.55mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量___(填“相等”或“不相等”),所求中和热____(填“相等”或“不相等”),简述理由___。
(4)若改用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会____(填“偏大”“偏小”或“无影响”)。
【答案】减少实验过程中的热量损失 偏小 不相等 相等 中和热是在稀溶液中,H+和OH-发生中和反应生成1 mol H2O时所放出的热量,与酸碱的用量无关 偏小
【解析】
(1)中和热测定需准确测定热量变化,尽可能防止热量损失;
(2)大烧杯上如不盖硬纸板,热量损失偏多;
(3)反应放出的热量和所用酸以及碱的量的多少有关;中和热是在稀溶液中,1 mol H+和1 mol OH-发生中和反应生成1 mol H2O时所放出的热量,与酸碱的用量无关;
(4)氨水是弱碱,电离吸热;
(1)中和热测定,尽可能防止热量损失,所以大小烧杯间填满碎泡沫塑料的作用是减少实验过程中的热量损失;
(2)大烧杯上如不盖硬纸板,热量损失偏多,求得的中和热数值将偏小;
(3)反应放出的热量和所用酸以及碱的量的多少有关,若用60 m L 0.50 mol·L-1盐酸与 50 m L 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,生成水的量不同,所放出的热量不相等,但因中和热是在稀溶液中,1 mol H+和1 mol OH-发生中和反应生成1 mol H2O时所放出的热量,与酸碱的用量无关,所求中和热相等;
(4)氨水是弱碱,电离吸热,若改用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会偏小。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是______________(填序号)。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:________________。
(3)如何用最简单的方法判断(1)中是否成功制备胶体?_________________________。
(4)取少量制得的胶体加入试管中,再加入少量(NH4)2SO4溶液,观察到的现象是__________,这种现象称为胶体的________________。
(5)Fe(OH)3胶体能稳定存在的主要原因是________(填序号)。
A. 胶粒直径小于1nm B. 胶粒带正电荷
C. 胶粒作布朗运动 D . 胶粒能透过滤纸
(6)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________(填序号)。
A.Fe(OH)3胶体粒子的直径在1~100nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
(7)向Fe(OH)3胶体中插入电极通电后,Fe(OH)3胶体粒子应该移向_______极,说明该胶体粒子带_____电;提纯Fe(OH)3胶体中混有的少量离子可以用的方法是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上合成氨反应的能量变化如图所示,该反应的热化学方程式是
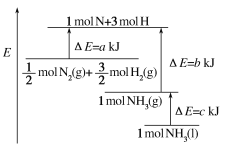
A. N2(g)+3H2(g)=2NH3(l) ΔH=2(a-b-c)kJ·mol-1
B. N2(g)+3H2(g)=2NH3(g) ΔH=2(b-a)kJ·mol-1
C. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
D. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组尝试在钢制钥匙上镀铜。
实验I:将钥匙直接浸入0.4 mol·L-1 CuCl2溶液中,20s后取出,钥匙表面变红,但镀层疏松,用纸即可擦掉。
实验II:用图装置对钥匙进行电镀铜。钥匙表面迅速变红,同时有细小气泡产生,精铜表面出现少量白色固体。30s后取出钥匙检验,镀层相对实验I略好,但仍能用纸巾擦掉一部分。经调整实验条件后获得了较好的电镀产品。
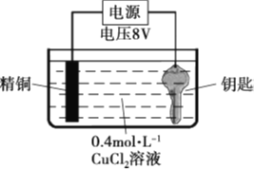
实验III:用0.4 mol·L-1 CuSO4溶液代替CuCl2溶液重复实验II,精铜表面未出现白色固体。
回答下列问题:
(1)实验I反应的化学方程式是_______。
(2)实验II中钥匙应与电源的_______极连接。
(3)钥匙表面产生的气体是_______。
(4)为了避免实验III中钥匙表面产生气体,应该采取的措施是________。
(5)常见化合物中铜元素有+1、+2两种价态,结合实验III推测实验II中精铜表面产生的白色固体的电极反应式是________。(已知CuOH是一种难溶于水的黄色固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼和氮的单质及一些化合物在工农业生产等领域有重要应用。回答下列问题:
(1)N原子核外有___ 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为____________________________。
(2)经测定发现,N2O5固体由NO2+和NO3-两种离子组成,该固体中N原子杂化类型为_________;与NO2+互为等电子体的微粒有_______(写出一种)。
(3)铵盐大多不稳定。NH4F、NH4I中,较易分解的是____,原因是__________________。
(4) 第二周期中,第一电离能介于B元素和N元素间的元素为_____(填“元素符号”)。
(5)晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体( 见图I),每个顶点为一个硼原子,每个三角形均为等边三角形。则每一个此基本结构单元由_______个硼原子构成;若该结构单元中有2 个原子为10B(其余为11B),那么该结构单元有_____种不同类型。

(6)硼和氮构成的一种氮化硼晶体的结构与石墨晶体结构相类似,B、N原子相互交替排列(见图II),其
晶胞结构如图III所示。设层内B-N核间距为apm,面间距为bpm,则该氮化硼晶体的密度为______g/cm3(用含a、b、NA 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A是气体单质,根据下图所示的A、B、C、D、E五种物质的相互转化关系,完成以下各题。
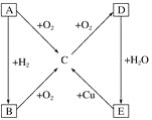
(1)分别写出下列物质的化学式
A______,B______,C______,D______,E______。
(2)写出有关反应的化学方程式:____________________________________________________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列电离方程式判断,下列分组正确的是( )
①H2SO4===2H++![]() 、②Ba(OH)2===Ba2++2OH-、③KAl(SO4)2===K++Al3++2
、②Ba(OH)2===Ba2++2OH-、③KAl(SO4)2===K++Al3++2![]() 、④NaHSO4===Na++H++
、④NaHSO4===Na++H++![]()
A. 属于酸的是①④ B. 属于碱的是②
C. 属于盐的只有③ D. 属于盐的只有④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是有机合成重要的中间体,其合成路线如图:
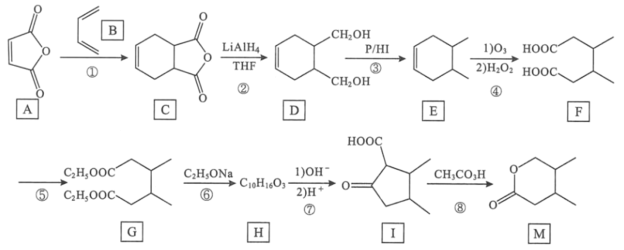
回答下列问题:
(1)B的名称为___。
(2)M中的官能团名称是___;④的反应类型为___。
(3)反应⑤所需的试剂和条件是___。
(4)反应⑥中的C2H5ONa仅提供碱性环境,则⑥的反应方程式为___。
(5)化合物D有多种同分异构体,符合下列条件的同分异构体共有___种(不考虑立体异构)。
①能与碳酸氢钠溶液反应放出气体;
②分子中含有六元环。
其中核磁共振氢谱有5组峰,且峰面积之比为1:2:3:4:4的结构简式为___。
(6)设计由乙烯和![]() 为原料制备
为原料制备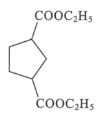 的合成路线___(无机试剂任选)。
的合成路线___(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4CO+2NO2![]() N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A. υ(CO)=1.5 mol·L-1·min-1 B. υ(NO2)=0.7 mol·L-1·min-1
C. υ(N2)=0.4 mol·L-1·min-1 D. υ(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com