
����Ŀ��(1)����ͼװ������������ʵ�飺
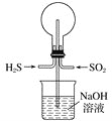
�ٳ����½�H2S��SO2�����ʵ���֮��Ϊ1��1������ƿ�����ã���ƿ���ܹ۲쵽��������_______��
������Cl2����SO2�������������䣬�۲쵽�����������֮ͬ��Ϊ______����֮ͬ��Ϊ_____�����ü�Ҫ���ֺͻ�ѧ����ʽ����ԭ�� ______��
������ʹ���з�Ӧ����ƿ�ڲ�������Ȫ�����������IJ���Ϊ________��
(2)ij����С��������ͼ��ʾװ�ý���ʵ�飺
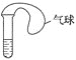
���Թ���ע��ij��ɫ��Һ�������Թܣ���Һ��Ϊ��ɫ����ȴ��ָ���ɫ�������Һ������_____��Һ������ʱ��Һ����ɫ��Ϊ��ɫ��ԭ����_______��
���𰸡�����ƿ�ڱ��ϸ����е���ɫ��������ƿ���γ���Ȫ ����ƿ�ڱ��ϸ����е���ɫ���� ��ƿ�в����γ���Ȫ Cl2��H2S��Ӧ��H2S��Cl2=S����2HCl����Ӧǰ���������û�б仯�����ܲ���ѹǿ����Բ����γ���Ȫ ����ë����ס��ƿ�������������ڵ�����ϳ�����ȥë��������Ȫ���� ����SO2��Ʒ�� SO2��Ʒ���γɵ����ʲ��ȶ�������ʱ�ֽ⣬SO2�����ݳ���Ʒ����Һ�ָ���ɫ
��������
(1)�ٳ����½�H2S��SO2�����ʵ���֮��Ϊ1��1������ƿ��2H2S+SO2=3S+2H2O�ݴ˷������
������Cl2����SO2�������������䣬 H2S��Cl2=S����2HCl���ݴ˷������
������HCl��������ˮ������ʹ���з�Ӧ����ƿ�ڲ�������Ȫ��������Ҫʹ��ƿ��������ˮ�Ӵ���ʹѹǿ��С���ݴ˷������
(2)���Թ���ע��ij��ɫ��Һ�������Թܣ���Һ��Ϊ��ɫ����ȴ��ָ���ɫ����϶�����������ʷ������
(1)�ٳ����½�H2S��SO2�����ʵ���֮��Ϊ1��1������ƿ��2H2S+SO2=3S+2H2O�����ú���ƿ�������ѹǿ��С���ܹ۲쵽����ƿ�ڱ��ϸ����е���ɫ��������ƿ���γ���Ȫ���ʴ�Ϊ������ƿ�ڱ��ϸ����е���ɫ��������ƿ���γ���Ȫ��
������Cl2����SO2�������������䣬Cl2����ǿ�����ԣ��ܹ���H2S��������S���ʣ�ͬʱ����HCl��H2S��Cl2=S����2HCl������ѹǿ���䣬�۲쵽�����������֮ͬ��Ϊ����ƿ�ڱ��ϸ����е���ɫ��������֮ͬ��Ϊ��ƿ�в����γ���Ȫ���ʴ�Ϊ������ƿ�ڱ��ϸ����е���ɫ��������ƿ�в����γ���Ȫ��Cl2��H2S��Ӧ��H2S��Cl2=S����2HCl����Ӧǰ���������û�б仯�����ܲ���ѹǿ����Բ����γ���Ȫ��
������HCl��������ˮ������ʹ���з�Ӧ����ƿ�ڲ�������Ȫ�����������IJ���Ϊ����ë����ס��ƿ�������������ڵ�����ϳ�����ȥë��������Ȫ�������ʴ�Ϊ������ë����ס��ƿ�������������ڵ�����ϳ�����ȥë��������Ȫ������
(2)���Թ���ע��ij��ɫ��Һ�������Թܣ���Һ��Ϊ��ɫ����ȴ��ָ���ɫ�������Һ����������SO2��Ʒ����Һ��SO2��Ʒ���γɵ����ʲ��ȶ�������ʱ�ֽ⣬SO2�����ݳ���Ʒ����Һ�ָ���ɫ����ȴ������������Ʒ���γɵIJ��ȶ�����ɫ���ʣ�Ʒ����Һ�ɺ�ɫ�����ɫ���ʴ�Ϊ������SO2��Ʒ�죻SO2��Ʒ���γɵ����ʲ��ȶ�������ʱ�ֽ⣬SO2�����ݳ���Ʒ����Һ�ָ���ɫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����[2��2]����Ľṹ��ʽ��ͼ�����й��ڸû������˵��������ǣ� ��

A.�뻷��ϩ��Ϊͬ���칹��B.���ȴ��ﳬ������
C.����̼ԭ�Ӳ���ƽ��D.����黥Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2molA��2molB�����2L���ܱ������У��������·�Ӧ��2A(g)+3B(g) ![]() 2C(g)+2D(g),2s��A��ת����Ϊ50%�����v(D)=0.25mol/(L��s)�������ƶϲ���ȷ����
2C(g)+2D(g),2s��A��ת����Ϊ50%�����v(D)=0.25mol/(L��s)�������ƶϲ���ȷ����
A. z=2
B. 2s�������ڵ�ѹǿ�dz�ʼ��7/8��
C. 2sʱ,C���������Ϊ2/7
D. 2s��B��Ũ��Ϊ0.5mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����( )
A.�������������������Һ�У� SiO2+4H++4F-=SiF4�� +2H2O
B.ƫ��������Һ��ͨ�������CO2��2AlO2- + CO2+3H2O=2Al(OH)3��+ CO32-
C.ϡ�����������������Һ�У�H+ +![]() + Ba2+ + OH-=BaSO4��+ H2O
+ Ba2+ + OH-=BaSO4��+ H2O
D.��������Һ�м�������İ�ˮ��Al3++3NH3��H2O=Al(OH)3��+3NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z�����ֳ���Ԫ�صĵ��ʣ��ס��������ֳ����Ļ������Щ���ʺͻ�����֮�������ͼ��ʾ��ת����ϵ����Ӧ�����ԣ�������˵������ȷ���ǣ�������
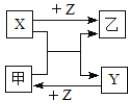
A.�ס������ֻ�����ֻ��ͨ�����Ϸ�Ӧ�õ�
B.X�ȿ����ǽ���Ԫ��Ҳ�����Ƿǽ���Ԫ��
C.���ڳ����£��ȿ�������̬Ҳ������Һ̬����̬
D.��X��Y�Ƿǽ���Ԫ�أ���ǽ�����X��Yǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10 mol��L-1 H2SO4���� 480mL 1mol��L-1 H2SO4�������¼���������
�ټ��㲢����Ͳ��ȡ x mL10 mol��L-1 H2SO4��ϡ�ͣ�
�ڽ�ϡ�ͺ����Һת����Ϊ y ������ƿ�У�
������������ˮϴ���ձ��Ͳ�����2�C3�Σ���ת������ƿ��
�ܼ���������ƿ�м�����ˮ���̶��ߣ�
�ݽ�����ƿ���������ҡ�ȡ�
(1)����д���������� x��y�ֱ��ǣ�x________________��y________________��
(2)��û�н��в����ۣ���������Һ��Ũ��________________ (�ƫ�ߡ�����ƫ�͡���Ӱ�족����ͬ)���������ж���ʱ���ӿ̶��ߣ���������Һ��Ũ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z����ͼ��ʾ��ת����ϵ����X��Y�����ǣ�������
��Si��SiO2 ��AlCl3��Al(OH)3��CuO��CuSO4 ��Fe��FeCl2
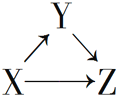
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������У���Ӧ3A(g)��B(s)![]() 2C(g)��2D(g) ��H >0�ﵽƽ��ı���������������˵����ȷ���ǣ� ��
2C(g)��2D(g) ��H >0�ﵽƽ��ı���������������˵����ȷ���ǣ� ��
A. ����ѹǿ�������淴Ӧ����ͬ�ȳ̶�����ƽ�ⲻ�ƶ�
B. �����¶ȣ�����Ӧ���������淴Ӧ���ʼ�С��ƽ�����������ƶ�
C. ����A��Ũ�ȣ�ƽ�����������ƶ���ƽ�ⳣ������
D. ����B�������������淴Ӧ���ʲ��䣬ƽ�ⲻ�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯���������ǵ���������֡�
��1������β����NO���ɹ��̵������仯ʾ��ͼ��ͼ��
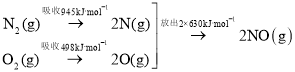
�������£�![]() ��
��![]() ��ȫ��Ӧ����
��ȫ��Ӧ����![]() ����___�����������������ų�����__kJ������
����___�����������������ų�����__kJ������
��2��һ���¶��£������Ϊ![]() �ĺ����ܱ������У�������̬������X��Y֮�䷴Ӧ�����и����ʵ����ʵ�����ʱ��Ĺ�ϵ��ͼ��ʾ��
�ĺ����ܱ������У�������̬������X��Y֮�䷴Ӧ�����и����ʵ����ʵ�����ʱ��Ĺ�ϵ��ͼ��ʾ��
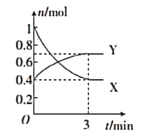
��д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��____�������ʵĻ�ѧʽ��ʾ��
����![]() �ڣ���Y��ʾ�ķ�Ӧ����Ϊ____��
�ڣ���Y��ʾ�ķ�Ӧ����Ϊ____��
������������˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����____������ĸ����
a.������ѹǿ���ٷ����仯
b.X������������ٷ����仯
c.������ԭ���������ٷ����仯
d.��ͬʱ��������![]() ��ͬʱ����
��ͬʱ����![]()
�ܷ�Ӧ�ﵽƽ����������¶ȣ���v������____��v���棩___����������������С����������������
��3����Ӧ![]() �����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
��![]() ��
��![]()
��![]() ��
��![]()
�÷�Ӧ�����ֲ�ͬ����������ɴ�С��˳��Ϊ���������գ�_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com