
| A、2HI(g)═H2(g)+I2(g)△H=+11kJ/mol | ||||
B、
| ||||
| C、H2(g)+I2(g)═2HI(g)△H=+288kJ/mol | ||||
D、
|
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于56.9 kJ |
| B、小于56.9 kJ |
| C、等于56.9 kJ |
| D、不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
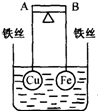 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )| A、杠杆为导体和绝缘体时,均为A端高B端低 |
| B、杠杆为导体和绝缘体时,均为A端低B端高 |
| C、当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低 |
| D、当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V(碱)=V(酸) |
| B、V(碱)=10V(酸) |
| C、V(碱)=100V(酸) |
| D、V(碱)=1000V(酸) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x=2 | ||
| B、参加反应的Fe2+全部做还原剂 | ||
| C、每生成1mol Fe3O4,反应转移的电子总数为4mol | ||
D、1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100 mL 0.5 mol?L-1的MgCl2溶液 |
| B、200 mL 0.25 mol?L-1的CaCl2溶液 |
| C、100 mL 1.0 mol?L-1的NaCl溶液 |
| D、200 mL 0.25 mol?L-1的HCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com