
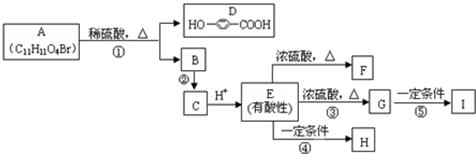
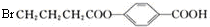 ,F为
,F为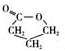 ,B为BrCH2CH2CH2COOH,根据E的结构可知,B在氢氧化钠水溶液、加热条件下发生水解反应生成C,则C的结构简式为:HOCH2CH2CH2COONa,C酸化得到E.E在浓硫酸作催化剂、加热条件下发生消去反应生成G,则G的结构简式为CH2=CHCH2COOH,G在一定条件下发生加聚反应生成I为
,B为BrCH2CH2CH2COOH,根据E的结构可知,B在氢氧化钠水溶液、加热条件下发生水解反应生成C,则C的结构简式为:HOCH2CH2CH2COONa,C酸化得到E.E在浓硫酸作催化剂、加热条件下发生消去反应生成G,则G的结构简式为CH2=CHCH2COOH,G在一定条件下发生加聚反应生成I为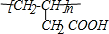 ,E在一定条件下发生缩聚反应生成H为:
,E在一定条件下发生缩聚反应生成H为: ,据此解答.
,据此解答.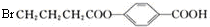 ,F为
,F为 ,B为BrCH2CH2CH2COOH,根据E的结构可知,B在氢氧化钠水溶液、加热条件下发生水解反应生成C,则C的结构简式为:HOCH2CH2CH2COONa,C酸化得到E.E在浓硫酸作催化剂、加热条件下发生消去反应生成G,则G的结构简式为CH2=CHCH2COOH,G在一定条件下发生加聚反应生成I为
,B为BrCH2CH2CH2COOH,根据E的结构可知,B在氢氧化钠水溶液、加热条件下发生水解反应生成C,则C的结构简式为:HOCH2CH2CH2COONa,C酸化得到E.E在浓硫酸作催化剂、加热条件下发生消去反应生成G,则G的结构简式为CH2=CHCH2COOH,G在一定条件下发生加聚反应生成I为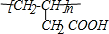 ,E在一定条件下发生缩聚反应生成H为:
,E在一定条件下发生缩聚反应生成H为: ,
,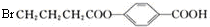 ,H的结构简式是
,H的结构简式是 ,
,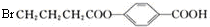 ;
; ;
; ,E中所含官能团的名称是:羧基、羟基,
,E中所含官能团的名称是:羧基、羟基, ;羧基、羟基;
;羧基、羟基;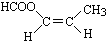 ,故答案为:
,故答案为: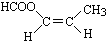 .
.


科目:高中化学 来源: 题型:
| A、减气空气进入量或增大天然气的进入量 |
| B、增大空气进入量或减小天然气的进入量 |
| C、减小空气进入量,同时减小天然气的进入量 |
| D、增大空气进入量,同时增大天然气的进入量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、放热44kJ |
| B、吸热22KJ |
| C、放热22kJ |
| D、吸热2.44KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用浓FeCl3溶液和NaOH溶液混合制备Fe(OH)3胶体 |
| B、将混有少量HCl的CO2通入饱和NaHCO3溶液中除去HCl |
| C、用湿润的pH试纸测定等浓度的Na2CO3和Na2SO3溶液的pH大小 |
| D、用AgNO3溶液鉴别Na2SO4溶液与NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
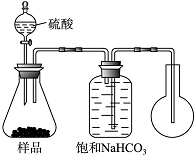 碳酸氢钠是一种在生产、生活实际中有着重要用途的化合物.某课外兴趣活动小组的同学进行了以下的实验活动.
碳酸氢钠是一种在生产、生活实际中有着重要用途的化合物.某课外兴趣活动小组的同学进行了以下的实验活动.| 温度/℃ | 10 | 20 | 30 | 加热煮沸后,冷却至50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
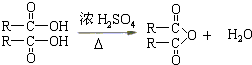
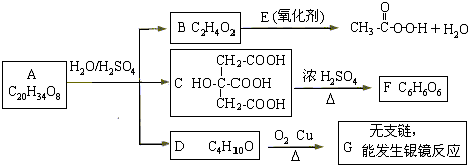
查看答案和解析>>
科目:高中化学 来源: 题型:
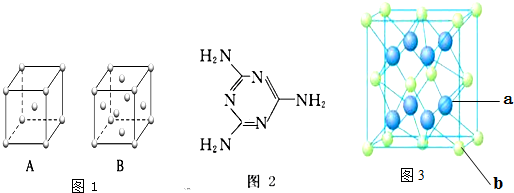
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+、Mg2+、NO3-、CO32- |
| B、Na+、Al3+、Cl-、AlO2- |
| C、Ba2+、K+、Cl-、HCO3- |
| D、NH4+、Fe3+、Ba2+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com