
| A�� | ��100 mL 1 mol•L-1�� Fe��NO3��3����Һ��ͨ������SO2��2Fe3++SO2+2H2O�T2Fe2++SO42-+4H+ | |
| B�� | ��100 mL 2 mol•L-1��FeI2����Һ��ͨ������5.6 L��Cl2��4Fe2++6I-+5Cl2�T4Fe3++3I2+10Cl- | |
| C�� | ��NaHCO3��Һ�м�������ij���ʯ��ˮ��2HCO3-+Ca2++2OH-�TCaCO3��+2H2O+CO32- | |
| D�� | ��������Һ�м������������������Һ��Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+AlO2-+2H2O |
���� A��©д��������ӷ�����������ԭ��Ӧ��
B��n��FeI2��=0.2mol��n��Cl2��=$\frac{5.6L}{22.4L/mol}$=0.25mol���ɵ����غ��֪��������ȫ�����������������Ӳ��ֱ�������
C��̼��������ȫ��Ӧ������̼��ơ�NaOH��ˮ��
D����Ӧ�������ᱵ��ƫ����غ�ˮ��
��� �⣺A����100 mL 1 mol•L-1�� Fe��NO3��3����Һ��ͨ������SO2�����ӷ�ӦΪ3NO3-+Fe3++5SO2+4H2O�T3NO��+Fe2++5SO42-+8H+����A����
B����100 mL 2 mol•L-1��FeI2����Һ��ͨ������5.6 L��Cl2�����ӷ�ӦΪ2Fe2++8I-+5Cl2�T2Fe3++4I2+10Cl-����B����
C����NaHCO3��Һ�м�������ij���ʯ��ˮ�����ӷ�ӦΪHCO3-+Ca2++OH-�TCaCO3��+H2O����C����
D����������Һ�м������������������Һ�����ӷ�ӦΪAl3++2SO42-+2Ba2++4OH-�T2BaSO4��+AlO2-+2H2O����D��ȷ��
��ѡD��
���� ���⿼�����ӷ�Ӧ����ʽ��д�������жϣ�Ϊ��Ƶ���㣬���շ����ķ�Ӧ�����ӷ�Ӧ����д����Ϊ���Ĺؼ������ظ��ֽⷴӦ��������ԭ��Ӧ�����ӷ�Ӧ���飬ע�����ӷ�Ӧ�б�����ѧʽ�����ʼ����ӡ�����غ㣬��Ŀ�ѶȲ���


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������K+��Mg2+��Fe2+��MnO4- | |
| B�� | NaOH��Һ�У�Cu2+��NH4+��SO42-��CO32- | |
| C�� | FeCl3��Һ�У�Al3+��Na+��I-��SO42- | |
| D�� | NaClO��Һ�У�K+��SO42-��OH-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ʯȼ�Ͽ��ɡ��ӹ����̳�����H2S������H2S��ת������Դ���úͻ�����������Ҫ���⣮
��ʯȼ�Ͽ��ɡ��ӹ����̳�����H2S������H2S��ת������Դ���úͻ�����������Ҫ���⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶ȡ�����ѹǿ�����ӵ��� | B�� | �����¶ȡ�����ѹǿ��������� | ||
| C�� | �����¶ȡ�����ѹǿ�����ӵ��� | D�� | �����¶ȡ�����ѹǿ����������ְ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��pH=4�Ĵ�����Һϡ�ͺ�H+Ũ������ | |
| B�� | �����£�0.01L pH=10��NaOH��Һ��ˮϡ�͵�10L����ʱ��Һ��pH=7 | |
| C�� | �ı�����ʹ����ĵ���ƽ�������ƶ�������ĵ����һ������ | |
| D�� | ������0.1mol•L-1������Һ��pH=a�����������Ĵ����ƹ�����ʹ��ҺpH=��a+1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��SO42-��CO32- | B�� | NH4+��Na+��SO42- | C�� | Mg2+��HCO3-��Cl- | D�� | Ag+��Al3+��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6�� | B�� | 4�� | C�� | 5�� | D�� | 3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
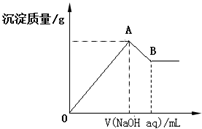
| A�� | x=$\frac{3a}{5-a}$ | |
| B�� | x��ȡֵ��Χ��0��x��$\frac{11}{32}$ | |
| C�� | A��������ֵ����x�����仯 | |
| D�� | ��B�������Ϊ200mLʱ��c��NaOH��=7.0mol/L |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com