
| A、0.1mol?L-1NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、0.1mol?L-1NH4Cl和0.1mol?L-1NH3?H2O等体积混合后离子浓度关系:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:c(Na+)=c(CH3COO-) |
| D、常温下,在pH=1的溶液中,Fe2+、NO3-、ClO-、Na+能大量共存 |


科目:高中化学 来源: 题型:
 将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol?L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )
将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol?L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )| A、A点所表示的沉淀是:Al(OH)3、BaSO4 |
| B、B-C段所发生反应的离子方程式是:H++OH-→H2O |
| C、A-B段发生反应的离子方程式:Ba2++SO42-→BaSO4↓ |
| D、拐点E的横坐标为70mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、其原子最外电子层只1个电子的元素 |
| B、最低负化合价为-3价的元素 |
| C、其原子最外层电子数大于电子层数的元素 |
| D、最高价氧化物对应的水化物是酸的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可用加热法除去氯化钠固体中的氯化铵杂质 |
| B、只用铜片不能鉴别浓硝酸和稀硝酸 |
| C、常温下,Al和浓硫酸钝化说明Al和浓硫酸在常温下不反应 |
| D、SO2通入氯化钡溶液无现象,若再通入NH3或NO2气体则都会产生BaSO4的白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
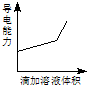 浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )| A | B | C | D | |
| 溶液(Ⅰ) | 盐酸 | 醋酸 | 氢氧化钠 | 氨水 |
| 溶液(Ⅱ) | 氢氧化钠 | 氢氧化钠 | 氨水 | 硝酸银 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4、NH3、H2O、三种分子的空间构型虽然不同,但中心原子的轨道杂化类型却相同 |
B、苯乙烯( )分子中的所有原子,不可能在同一平面内 )分子中的所有原子,不可能在同一平面内 |
| C、质谱仪可以测定有机化合物的相对分子质量 |
| D、红外光谱可以反映有机化合物中化学键或者官能团的相关信息 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:9 | B、1:11 |
| C、9:1 | D、11:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com