
【题目】下列关于常见有机物的说法正确的是
A. 淀粉水解与纤维素水解得到的最终产物不相同
B. 蛋白质、纤维素、蔗糖、油脂都是高分子化合物
C. 乙酸和油脂都能与NaOH溶液反应
D. 乙醇、乙酸和乙酸乙酯不能用饱和Na2CO3溶液鉴别
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A. 向KI溶液中通入适量Cl2后,溶液颜色变深
B. 向KCl溶液中滴加几滴酚酞溶液,溶液颜色变红
C. 溴水与NaCl溶液混合时,会发生置换反应
D. NaCl溶液在空气中会被氧化,故需要密封保存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类正确的是( )
A. 混合物:水玻璃、碱石灰、明矾 B. 酸:稀硫酸、次氯酸、硫酸氢钠
C. 酸性氧化物:SO2、CO2、SiO2 D. 碱性氧化物:CaO、Na2O2、K2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积可变的恒压容器中,反应2NO2(g)N2O4(g)达到平衡后,再向容器内通入一定量NO2,再次达到平衡时,N2O4的体积分数( )
A.不变 B.增大 C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。设X的原子序数为a,则下列说法不正确的是

A. Y的原子序数可能为a-17
B. Y与Z的原子序数之和可能为2a
C. Z的原子序数可能为a+31
D. X、Y、Z一定为短周期元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
I.2015年国产C919大型客机正式下线,标志着我国成为世界上少数几个具有自行研制大型飞机的国家之一,标志着我国航空工业进入了新的发展阶段。
(1)飞机的外壳通常采用镁-铝合金材料,铝的价电子排布图为 ,第一电离能:镁 (填“大于”或“小于”)铝。
(2)现代飞机为了减轻质量而不减轻外壳承压能力,通常采用复合材料--玻璃纤维增强塑料,其成分之一为环氧树脂,常见的E51型环氧树脂中部分结构如下图所示:
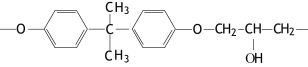

其中碳原子的杂化方式为 ,个数比为 。
II.大型飞机的发动机被誉为航空工业皇冠上的“宝石”。制造过程中通常采用碳化钨做关键部位的材料。
(3)钨元素位于周期表的第六周期第VIB族,请写出其外围电子排布式 ;
(4)下图为碳化钨晶体的一部分结构, 碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有 个,1个钨原子周围距离钨原子最近的碳原子有 个 ,下列金属元素的堆积方式与碳化钨晶胞中碳原子和钨原子所处位置类似的是 。
A. Fe Cu B.Ti Au C.Mg Zn D.Cu Ag
(5)假设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g/mol,密度为b g/cm3,则阿伏加德罗常数NA用上述数据可以表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 甘氨酸和丙氨酸缩合只能形成一种二肽
B. 醋酸铅溶液可使蛋白质发生盐析
C. 三大合成材料为塑料、合成纤维、合成橡胶
D. 油脂属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的无机物的转化关系中,部分生成物和反应条件已略去。其中A与F是两种酸式盐;常温下B、C、Y、Z是气体,且B能使Z的水溶液褪色;E是一种常见的化肥;X中含有20个电子。

(1)写出X的电子式:________________ ;E中含有的化学键类型是________________。
(2)Z与C以物质的量之比31反应也能生成G,同时生成另一种二元化合物H,已知该反应 中只有一种元素的化合价发生改变,则H的化学式为________________。H大量用于面粉的漂白和消毒,它与水反应的化学方程式为________________。
(3)将体积均为560 mL(标准状况)的B和Z同时缓缓通入水中,得到1.0 L溶液,则溶液中c(H + )=________mol/L。
(4)A~G七种物质中,属于电解质的有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.
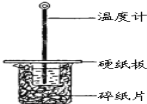
(1)下列说法不正确的是( )
A.该实验也可在保温杯中进行
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是保温、隔热,减少热量损失
D.若将盐酸体积改为60mL,两次实验所求得中和热不相等
(2)若通过实验测定中和热的△H的绝对值常常小于57.3kJ/mol,其原因可能是_________
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
C.量取NaOH溶液的体积时仰视读数
D.用温度计测定盐酸初始温度后,直接测定氢氧化钠溶液的温度
(3)将一定量的稀氨水、稀氢氧化钠溶液、稀氢氧化钡溶液分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为__________;

(4)若将V1mL1.0molL-1 HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).由图2可知,氢氧化钠的浓度为 __________ ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com