
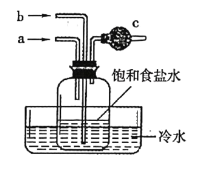
【题目】用如图所示的实验装置模拟侯氏制碱法的主要反应原理。下列说法正确的是
A.侯氏制碱法中可循环利用的气体为![]()
B.先从a管通入NH3,再从b管通入CO2
C.为吸收剩余的NH3,c中应装入碱石灰
D.反应后冷却,瓶中析出的晶体主要是纯碱
【答案】B
【解析】
侯氏制碱法的原理:
①将足量NH3通入饱和食盐水中,再通入CO2,溶液中会生成高浓度的HCO3-,与原有的高浓度Na+结合成溶解度较小的NaHCO3析出:NaCl+NH3+CO2+H2O![]() NaHCO3↓+NH4Cl;
NaHCO3↓+NH4Cl;
②将析出的沉淀加热,制得Na2CO3(纯碱):2NaHCO3![]() Na2CO3+CO2↑+H2O,生成的CO2可用于上一步反应(循环利用);
Na2CO3+CO2↑+H2O,生成的CO2可用于上一步反应(循环利用);
③副产品NH4Cl可做氮肥。
A.侯氏制碱法中可循环利用的气体是CO2,A项错误;
B.先通入NH3,NH3在水中的溶解度极大,为了防止倒吸,应从a管通入,之后再从b管通入CO2,B项正确;
C.碱石灰(主要成分是NaOH和CaO)不能吸收NH3,C项错误;
D.反应后冷却,瓶中析出的晶体主要是NaHCO3,将其加热得到纯碱(Na2CO3),D项错误;
答案选B。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】2019年诺贝尔奖授予JohnB.Goodenough等三位科学家,以表彰其在锂电池领域的贡献。磷酸亚铁锂(LiFePO4)用作锂离子电池正极材料,制备方法如图:

(1)制备水合磷酸铁(FePO4·xH2O)固体
①过程Ⅰ,加NaOH溶液调pH=2.0时透明混合溶液中含磷微粒主要是H2PO4-,过程Ⅰ发生的主要离子方程式是____。
②过程Ⅱ“氧化、沉淀”反应生成FePO4沉淀的离子方程式是____。
③进行过程III之前,需确认过程II中无Fe2+,检验试剂为____。
④FePO4·xH2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图:

水合磷酸铁的化学式为____。(x取整数)
(2)制备LiFePO4固体:
在氮气气氛保护下,高温焙烧FePO4、Li2CO3和过量葡萄糖的固体混合物。
①过量葡萄糖作用是____。
②锂离子电池在充电时,电极材料LiFePO4会迁出部分Li+,部分转变为Li(1-x)FePO4。此电极的电极反应为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茚地那韦被用于新型冠状病毒肺炎的治疗,其结构简式如图所示(未画出其空间结构)。

下列说法正确的是( )
A.茚地那韦属于芳香族化合物,易溶于水
B.虚线框内的所有碳、氧原子均处于同一平面
C.茚地那韦可与氯化铁溶液发生显色反应
D.茚地那韦在碱性条件下完全水解,最终可生成三种有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有的氯化镁是镁的重要来源之一。从海水中制取镁有多种生产方法,可按如下步骤进行:
①把贝壳制成石灰乳
②在引入的海水中加石灰乳,沉降、过滤、洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤、干燥产物
④将得到的产物熔融后电解
关于从海水中提取镁的下列说法不正确的是( )
A. 此法的优点之一是原料来源丰富
B. 进行①②③步骤的目的是从海水中提取氯化镁
C. 以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应
D. 第④步电解制镁是由于镁是很活泼的金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(化合物L)是人们熟知的解热镇痛药物。一种长效、缓释阿司匹林(化合物P)的合成路线如图所示:

已知:①HC![]() CH+RCOOH
CH+RCOOH![]() RCOOCH=CH2
RCOOCH=CH2
②RCOOR’+R”OH![]() RCOOR”+R’OH
RCOOR”+R’OH
(1)B中的官能团是__。
(2)C的结构简式是__。
(3)D→E的反应类型是__。
(4)E→G的化学方程式是__。
(5)已知:H是芳香族化合物。在一定条件下2B→K+H2O,K的核磁共振氢谱只有一组峰。J→L的化学方程式是__。
(6)L在体内可较快转化为具有药效的J,而P与L相比,在体内能缓慢持续释放J。
①血液中J浓度过高能使人中毒,可静脉滴注NaHCO3溶液解毒。请用化学方程式解释NaHCO3的作用:__。
②下列说法正确的__(填字母)。
a.P中的酯基在体内可缓慢水解,逐渐释放出J
b.P在体内的水解产物中没有高分子化合物
c.将小分子药物引入到高分子中可以实现药物的缓释功能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式为 ,下列叙述不正确的是( )
,下列叙述不正确的是( )
A. 1mol该有机物在加热和催化剂作用下,最多能和4 molH2反应
B. 该有机物能使溴水褪色也能使酸性KMnO4溶液褪色
C. 该分子中最多有9个碳原子共平面
D. 该有机物在一定条件下,能发生消去反应或取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性强弱:I- >Fe2+>Br-,向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这三种离子的物质的量随消耗氯气物质的量的变化如图所示。下列说法中正确的是
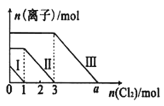
A.a值等于6
B.线段Ⅰ代表Br-的变化情况
C.线段Ⅲ代表Fe2+的变化情况
D.原混合溶液中n(FeBr2)=4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种由明矾石[主要成分:KAl3(SO4)2(OH)6]和地开石[主要成分:Al4(Si4O10)(OH)8]提取K2SO4和Al的工艺流程:

已知:K2SO4在不同温度下的溶解度
温度/℃ | 10 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 9.3 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
回答下列问题:
(1)硫酸熟化工艺是指浓硫酸在矿物颗粒表面均匀分布并向内扩散的过程,该过程中矿物颗粒_____(填“是”或“不是”)越细越好。
(2)完成并配平还原焙烧时明矾石与硫反应的化学方程式:________
![]() KAl3(SO4)2(OH)6+
KAl3(SO4)2(OH)6+![]() S→
S→![]() K2SO4+
K2SO4+![]() Al2O3+
Al2O3+![]() ___________+
___________+![]() H2O
H2O
(3)从水浸后的滤液中得到K2 SO4晶体的操作a是 _____,写出K2SO4的一种用途 _____ .
(4)碱浸过程中发生的主要反应的离子方程式为____、 ____ 。
(5)流程中制Al的化学方程式为________________________
(6)现利用还原焙烧产生的SO2来生产硫酸。若明矾石的质量为41.4t,主要成分含量为50%,SO2的利用率为96%,则可生产质量分数为98%的硫酸____t。[KAl3(SO4)2(OH)6的相对分子质量为414]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平)。
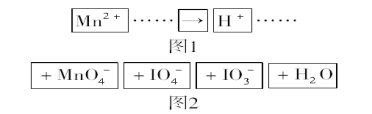
对该氧化还原反应型离子方程式,说法不正确的是( )
A.IO4-作氧化剂具有氧化性
B.氧化剂和还原剂的物质的量之比为5∶2
C.若有2molMn2+参加反应时则转移10mol电子
D.氧化性:MnO4->IO4-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com