
【题目】一种由明矾石[主要成分:KAl3(SO4)2(OH)6]和地开石[主要成分:Al4(Si4O10)(OH)8]提取K2SO4和Al的工艺流程:

已知:K2SO4在不同温度下的溶解度
温度/℃ | 10 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 9.3 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
回答下列问题:
(1)硫酸熟化工艺是指浓硫酸在矿物颗粒表面均匀分布并向内扩散的过程,该过程中矿物颗粒_____(填“是”或“不是”)越细越好。
(2)完成并配平还原焙烧时明矾石与硫反应的化学方程式:________
![]() KAl3(SO4)2(OH)6+
KAl3(SO4)2(OH)6+![]() S→
S→![]() K2SO4+
K2SO4+![]() Al2O3+
Al2O3+![]() ___________+
___________+![]() H2O
H2O
(3)从水浸后的滤液中得到K2 SO4晶体的操作a是 _____,写出K2SO4的一种用途 _____ .
(4)碱浸过程中发生的主要反应的离子方程式为____、 ____ 。
(5)流程中制Al的化学方程式为________________________
(6)现利用还原焙烧产生的SO2来生产硫酸。若明矾石的质量为41.4t,主要成分含量为50%,SO2的利用率为96%,则可生产质量分数为98%的硫酸____t。[KAl3(SO4)2(OH)6的相对分子质量为414]
【答案】不是 4KAl3(SO4)2(OH)6+3S===2K2SO4+6Al2O3+9SO2↑+12H2O 蒸发结晶 作钾肥、制备钾盐、药物、玻璃、明矾等 Al2O3+2OH-===2AlO2-+H2O SiO2+2OH-===SiO32-+H2O 2Al2O3(熔融)![]() 4Al+3O2↑ 10.8
4Al+3O2↑ 10.8
【解析】
由工艺流程可知,地开石、明矾石经硫酸熟化后加入硫单质进行还原焙烧,明矾石发生反应4KAl3(SO4)2(OH)6+3S=2K2SO4+6Al2O3+9SO2↑+12H2O,地开石发生反应Al4(Si4O10)(OH)8=4SiO2+2Al2O3+4H2O,焙砂的主要成分为K2SO4、SiO2和Al2O3,再通过水浸后得到水浸出液K2SO4溶液和水浸出渣SiO2、Al2O3,结合K2SO4的溶解度随温度的变化可知,K2SO4溶液经蒸发结晶得到K2SO4晶体,水浸出渣Al2O3与SiO2分别与NaOH发生反应生成NaAlO2和Na2SiO3,再经一些列操作得到Al单质,据此分析解答问题。
(1)矿物颗粒细,可以提高扩散速率,但颗粒细度达到一定值后,再往后对速率的影响微乎其微,因此,硫酸熟化过程中矿物颗粒不是越细越好,故答案为:不是;
(2)根据上述分析,明矾石与硫发生氧化还原反应,硫作还原剂,KAl3(SO4)2(OH)6作氧化剂,根据氧化还原反应得失电子守恒进行配平可得,化学反应方程式为4KAl3(SO4)2(OH)6+3S=2K2SO4+6Al2O3+9SO2↑+12H2O,故答案为:4KAl3(SO4)2(OH)6+3S=2K2SO4+6Al2O3+9SO2↑+12H2O;
(3)K2SO4的溶解度虽然随着温度的升高而增大,但是变化不大,因此K2SO4溶液可采用蒸发结晶得到K2SO4晶体。K2SO4可用作钾肥,制加盐、药物、玻璃、明矾等,故答案为:蒸发结晶;作钾肥、制备钾盐、药物、玻璃、明矾等;
(4)碱浸过程中,主要是Al2O3与SiO2分别与NaOH发生反应,生成NaAlO2和Na2SiO3,离子反应方程式为Al2O3+2OH-===2AlO2-+H2O;SiO2+2OH-===SiO32-+H2O;故答案为:Al2O3+2OH-===2AlO2-+H2O;SiO2+2OH-===SiO32-+H2O;
(5)流程中制备Al可采用电解熔融Al2O3的方法,发生的化学反应方程式2Al2O3(熔融)![]() 4Al+3O2↑,故答案为:2Al2O3(熔融)
4Al+3O2↑,故答案为:2Al2O3(熔融)![]() 4Al+3O2↑;
4Al+3O2↑;
(6)根据明矾石与硫反应方程式和元素守恒可得关系式:

则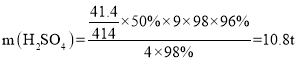 ,故答案为:10.8。
,故答案为:10.8。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是
A. 当它们的体积和温度、压强均相同时,三种气体的密度ρ(H2)>ρ(N2)>ρ(O2)
B. 当它们的温度和密度都相同时,三种气体的压强p(H2)<p(N2)<p(O2)
C. 当它们的质量和温度、压强均相同时,三种气体的体V(O2)<V(N2)<V(H2)
D. 当它们的压强和体积、温度均相同时,三种气体的质量m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示的实验装置模拟侯氏制碱法的主要反应原理。下列说法正确的是
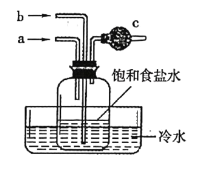
A.侯氏制碱法中可循环利用的气体为![]()
B.先从a管通入NH3,再从b管通入CO2
C.为吸收剩余的NH3,c中应装入碱石灰
D.反应后冷却,瓶中析出的晶体主要是纯碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种副作用小的新型镇痛消炎药K的合成路线如图所示:
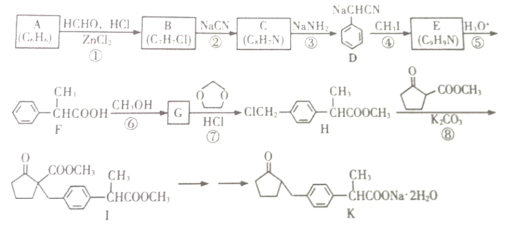
请回答下列问题
(1)F分子中官能团的名称为______________;B分子中处于同一平面的原子最多有____个
(2)反应⑥的条件为_______________;反应⑧的类型为_______________________。
(3)反应⑦除生成H外,另生成一种有机物的结构简式为_______________________。
(4)反应①的化学方程式为_______________________。
(5)符合下列条件的G的同分异构体有_____________种
Ⅰ.苯环上有且仅有四个取代基;
Ⅱ.苯环上的一氯代物只有一种;
Ⅲ.能发生银镜反应。
其中还能发生水解反应的同分异构体的结构简式为______________(只写一种即可)。
(6)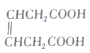 是合成
是合成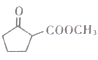 的重要中间体。参照题中合成路线,设计由1,3-丁二烯合成
的重要中间体。参照题中合成路线,设计由1,3-丁二烯合成![]() 的一种合成路线(无机试剂任选):_______________。
的一种合成路线(无机试剂任选):_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 能电离出H+的化合物除水外都是酸,分子中含有几个氢原子它就是几元酸
B. 无机含氧酸分子中含有几个羟基,它就属于几元酸
C. 同一元素的含氧酸,该元素的化合价越高,其酸性越强,氧化性也越强
D. H3PO4和H2CO3分子中非羟基氧的个数均为1,但它们的酸性不相近,H3PO4是中强酸而H2CO3是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某相对分子质量小于200的芳香族含氧衍生物中氧的质量分数约为13.1%(仅含碳、氢、氧三种元素),已知其分子中含有2个-CH3,且该物质遇FeCl3溶液显紫色,则该有机物的结构式共有
A. 2种B. 4种C. 6种D. 8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:

(1)b极上的电极反应式为__,甲电池的总反应化学方程式是__。
(2)在粗铜的电解过程中,图中c电极的材料是__(填“粗铜板”或“纯铜板”);在d电极上发生的电极反应为__;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是__,电解一段时间后,电解液中的金属离子有__。
(3)如果要在铁制品上镀镍(二价金属,相对原子质量59),则f电极的材料是__(填“铁制品”或“镍块”,下同),e电极的材料是__。
(4)若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气的用途非常广泛。实验室用如下装置制取氯气,并用制取氯气进行性质探究实验。回答下列问题:
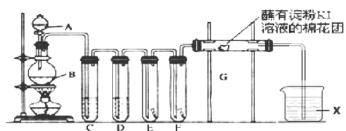
(1)A中盛有浓盐酸,B中盛有![]() ,写出反应的离子方程式__________________。
,写出反应的离子方程式__________________。
(2)E中为红色干布条,F中为红色湿布条,对比E和F中观察现象的差异可得出的结论是__________________。
(3)试管C和D中试剂名称各为_____________________。X试剂的作用是______________。
(4)装置G处发生反应的离子方程式为_____________________________。
(5)家庭中常用消毒液(主要成分![]() )与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

①“与洁厕灵同时使用”会产生有毒氯气,写出反应的离子方程式____________。
②需“密闭保存”的原因_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修5:有机化学基础](15分)聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景。 PPG的一种合成路线如下:
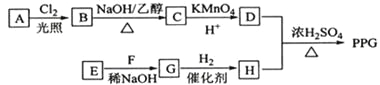
已知:
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为单氯代烃:化合物C的分子式为C5H8;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④![]() 。
。
回答下列问题:
(1)A的结构简式为 。
(2)由B生成C的化学方程式为 。
(3)由E和F生成G的反应类型为 ,G的化学名称为 。
(4)①由D和H生成PPG的化学方程式为 。
②若PPG平均相对分子质量为10000,则其平均聚合度约为 (填标号)。
a.48 b.58 c.76 d.122
(5)D的同分异构体中能同时满足下列条件的共有 种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体
②既能发生银镜反应,又能发生皂化反应
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 (写结构简式):
D的所有同分异构体在下列—种表征仪器中显示的信号(或数据)完全相同,该仪器是_____(填标号)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com