
【题目】下列对同系物归纳错误的是
A. 同系物都符合同一通式
B. 同系物彼此在组成上相差一个或若干个某种原子团
C. 同系物具有相同的最简式
D. 同系物的结构相似
科目:高中化学 来源: 题型:
【题目】100℃时,水的离子积为1×10-12 mol2·L-2,若该温度下某溶液中的H+浓度为1×10-7 mol·L-1,则该溶液是
A. 酸性 B. 中性 C. 碱性 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
A.常温常压下,18 g重水(D2O)所含的中子数为10NA
B.100℃时,1L pH=1的硫酸溶液中,含有0.2NA个H+
C.71g氯气发生氧化还原反应,一定失去2NA个电子
D.室温下,14gN2和CO的混合气体中含有的原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多个氨基酸分子缩合成2条肽链的蛋白质时,一共脱下49个水分子,由此推知,蛋白质分子含有的肽键数是
A. 50 B. 47 C. 49 D. 48
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H6)又称联氨,是一种可燃性的液体,可用作火箭燃料。
(1)101kPa,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼—空气燃料电池放电时其负极的电极反应式是 。
(3)如右图是一个电化学过程示意图。
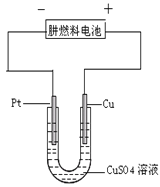
①铂片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程的电源,铜片质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气的体积含量为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是( )
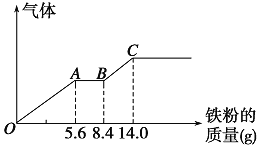
A.H2SO4浓度为2.5 mol·L-1
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.原混合酸中NO![]() 物质的量为0.1 mol
物质的量为0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素在周围表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A. 同一元素不可能既表现金属性,又表现非金属性
B. 第三周期主族元素的最高正化合价等于它所处的主族序数
C. 短周期元素形成离子后,最外层都达到8电子稳定结构
D. 同一主族的元素的原子,最外层电子数相同,化学性质完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种常用金属,镓(Ga)的化合物氮化镓(GaN)是制造LED的重要材料,被誉为第三代半导体材料。
I.镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似。
(1)Ga的原子结构示意图为___________________;
(2) GaN可由Ga和NH3在高温条件下制取,该反应的化学方程式_______________。
(3)下列有关镓和镓的化合物的说法正确的是____________
A.常温下,Ga可与水剧烈反应放出氢气
B.一定条件下,Ga可溶于盐酸和氢氧化钠
C.一定条件下,Ga2O3可与NaOH反应生成盐
D.Ga2O3可由Ga(OH)3受热分解得到
II.锌的冶炼方法有火法和湿法。工业上利用锌焙砂(主要含Zn0、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)湿法制取金属锌的流程如图所示:

已知:Fe的活泼性强于Ni
(4)ZnFe2O4可以写成ZnO·Fe2O3,ZnFe2O4与H2SO4反应的化学方程式为____ _。
(5)净化I操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,只使Fe3+转化为Fe(OH)3沉淀。净化I生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是________________________。
(6)净化II中加入Zn的目的是_______________________。
(7)常温下,净化I中,如果要使c(Fe3+) < 10-5 mol/L,则应控制溶液pH的范围为_____________。已知:Ksp[Fe(OH)3]=8.0×10-38;lg5=0.7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com