
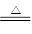 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O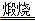 Na2CO3+H2O↑+CO2↑
Na2CO3+H2O↑+CO2↑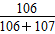 ×100%=49.77%
×100%=49.77%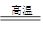 CaO+CO2↑CO2+NH3+H2O=NH4HCO3,
CaO+CO2↑CO2+NH3+H2O=NH4HCO3,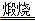 Na2CO3+H2O↑+CO2↑,
Na2CO3+H2O↑+CO2↑,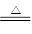 CaCl2+2NH3↑+2H2O,该反应的CaCl2中的Cl-来源于NaCl,Ca2+来源于CaCO3,产生无用的CaCl2,降低了NaCl的利用率。
CaCl2+2NH3↑+2H2O,该反应的CaCl2中的Cl-来源于NaCl,Ca2+来源于CaCO3,产生无用的CaCl2,降低了NaCl的利用率。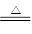 Na2CO3+H2O↑+CO2↑。
Na2CO3+H2O↑+CO2↑。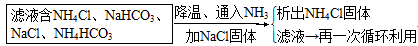
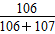 ×100%=49.77%。
×100%=49.77%。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.碳酸钠的热稳定性比碳酸氢钠强 |
| B.相同温度时,碳酸钠的溶解度大于碳酸氢钠 |
| C.同温度、同物质的量浓度时,碳酸钠溶液碱性大于碳酸氢钠溶液 |
| D.碳酸氢钠一定条件下可转化为碳酸钠,但碳酸钠不能转化为碳酸氢钠 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.隔绝空气加热,冷却后,称量剩余固体质量m1g |
| B.与足量稀盐酸反应并蒸干,称量剩余固体质量m2g |
| C.与足量水反应并加热,收集到标准状况下V1L干燥气体 |
| D.与足量稀硫酸反应并加热,收集到标准状况下V2L干燥气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
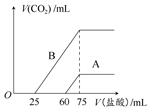
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
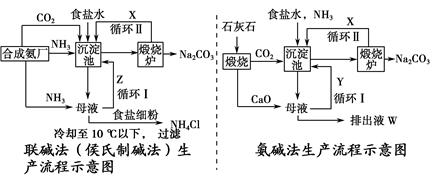
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.往两者饱和溶液中通入CO2,最终会形成澄清溶液的是NaHCO3 |
| B.除去碳酸氢钠固体中混有的少量碳酸钠可以采用加热的方法 |
| C.碳酸钠与盐酸反应放出二氧化碳的剧烈程度强于碳酸氢钠 |
| D.二者配成溶液,再加入石灰水,无白色沉淀生成的是NaHCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属钠在空气中燃烧的火焰呈黄色,是因为生成的Na2O2为淡黄色固体 |
| B.铁丝在Cl2中燃烧有红棕色的烟,是因为生成的FeCl3为红棕色固体 |
| C.过量的铁加入稀HNO3,充分反应后,滴入KSCN溶液,溶液呈红色,说明稀HNO3将Fe氧化为Fe3+ |
| D.取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
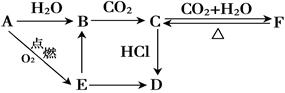
 C: ,
C: , B: ,
B: , F: 。
F: 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com