
 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。
3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。| | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 一定温度下氢气能还原氧化铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁表面形成致密氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
 Fe(OH)3+3H+(2分);酸性条件抑制了铁离子的水解,无法生成氢氧化铁胶体,不能使悬浮物沉降除去(2分)
Fe(OH)3+3H+(2分);酸性条件抑制了铁离子的水解,无法生成氢氧化铁胶体,不能使悬浮物沉降除去(2分)

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3︰1 | B.1︰2 | C.2︰1 | D.1∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

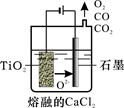
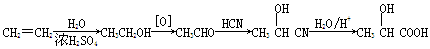
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入粉末质量/g | 13.68 | 27.36 | 34.20 |
| 生成气体的体积(标准状况)/L | 2.912 | 5.824 | 6.720 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2O3 | B.Fe3O4 | C.Fe4O5 | D.Fe5O7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
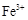 和
和 浓度相等。则已反应的
浓度相等。则已反应的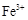 和未反应的
和未反应的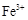 的物质的量之比是
的物质的量之比是| A.2︰3 | B.3︰2 | C.1︰2 | D.1︰1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将FeCl3溶液加热蒸干得到FeCl3固体 |
| B.向Fe(NO3)2溶液中加少量盐酸,无明显现象 |
| C.向氢氧化镁悬浊液中滴加FeCl3溶液,无明显现象 |
| D.向FeSO4溶液中滴加NaOH溶液,先出现白色沉淀,最终沉淀转化成红褐色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com