
����Ŀ���ס��ҡ�������������������ڵ����ʼ�������ͼ��ʾ����������������ݻ���ȣ��¶���ͬ����Ӧ�мס������ݻ����䣬���е�ѹǿ���䣬��һ���¶��·�Ӧ�ﵽƽ�⡣����˵����ȷ����
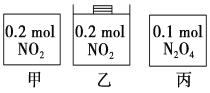
A��ƽ��ʱ��������c��NO2���Ĵ�С˳��Ϊ��>��>��
B��ƽ��ʱN2O4�İٷֺ�������>�ף���
C��ƽ��ʱ����NO2�����N2O4��ת������ͬ
D��ƽ��ʱ������ƽ����Է�����������>��>��
���𰸡�B
��������
����������ס��Ҵ���ƽ��2NO2N2O4���÷�ӦΪ�������ʵ�����С�ķ�Ӧ���ʼ���ѹǿ��С������ѹǿ���䣬���е����ƽ���൱���ڼ�ƽ��Ļ���������ѹǿ�����д���ƽ��N2O42NO2���൱�ڿ�ʼ����2molNO2�����Ϊ��Чƽ����A�������Ϊ��ȫ��Чƽ�⣬ƽ��ʱNO2Ũ�ȵ���ȣ����е����ƽ���൱���ڼ�ƽ��Ļ���������ѹǿ������ѹǿƽ��������Ӧ�ƶ�����ƽ���ƶ��Ľ���ǽ���NO2Ũ����������������ƽ��ʱ������c��NO2���Ĵ�С˳��Ϊ�ң���=������A����B�������Ϊ��ȫ��Чƽ�⣬ƽ��ʱN2O4�İٷֺ�����ȣ����е����ƽ���൱���ڼ�ƽ��Ļ���������ѹǿ������ѹǿƽ��������Ӧ�ƶ���ƽ��ʱN2O4�İٷֺ�������ƽ��ʱN2O4�İٷֺ������ң���=������B��ȷ��C�������Ϊ��ȫ��Чƽ�⣬ƽ��ʱ�ס�����N2O4�����ʵ�����ȣ���0.2��=0.1��1-��������æ�=1/3����ƽ��ʱ����NO2 �����N2O4 ��ת���ʿ�����ͬ����C����D�������Ϊ��ȫ��Чƽ�⣬ƽ��ʱ��������ƽ��Ħ��������ȣ����е����ƽ���൱���ڼ�ƽ��Ļ���������ѹǿ������ѹǿƽ��������Ӧ�ƶ����ܵ����ʵ�����С������ƽ��Ħ��������ã���ƽ��ʱ������ƽ����Է����������ң���=������D��������ѡB��


 ��ѧ��������������Ͼ���ѧ������ϵ�д�
��ѧ��������������Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ˮ��Һ�еĵ��뷽��ʽ��д��ȷ����( )
A��KClO3��K++3O2��+Cl5+ B��NaHCO3 �� Na++H++CO32��
C��H2SO4��H++ SO42�� D��Al2(SO4)3 �� 2Al3++3SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���CH3-C��C-CH2-CH3��˵������ȷ���ǣ�������
A. ������ֻ�зǼ��Լ���û�м��Լ�
B. ���������е�̼ԭ�Ӷ���ͬһ��ֱ����
C. �ܷ����ӳɷ�Ӧ
D. ���ܷ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���Ա������һ�֡�ˮ����أ����ܷ�ӦΪ��5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl����ͼ�á�ˮ�����Ϊ��Դ���NaCl��Һ��ʵ���У�X�缫������ɫ�����ݳ��������йط�����ȷ���ǣ� ��
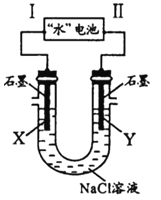
A��IΪ��������缫��ӦʽΪAg+Cl-+e-=AgCl
B����ˮ�������Na+�������������ƶ�
C��ÿת��1mole-��U��������0.5molH2O
D����ˮ������ڣ�ÿ����1molNa2Mn5O10��X�缫������1mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������������У���ȷ���ǣ���
A. ȡ��Na2CO3��Һʱ������ȡ�����࣬Ϊ�˲��˷ѣ��ְѹ������Լ������Լ�ƿ��
B. ���ܽ⡢���˵ķ��������Ȼ��ƺ�����صĻ����
C. ����NaOH���壬������ƽ�����ϷŴ�С���ֽƬ��Ȼ��NaOH��������ֽƬ�ϳ���
D. ���ö����ЧӦ����������Һ�ͽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ˮʱ��Һ�¶Ƚ��ͣ������½�1 mol��ɫ����ͭ�Ƴ���Һʱ�ų�����ΪQ1����֪�����ֽ���Ȼ�ѧ����ʽΪCuSO4��5H2O(s) ![]() CuSO4(s)��5H2O(l) ��H����Q2����Q1��Q2�Ĺ�ϵΪ
CuSO4(s)��5H2O(l) ��H����Q2����Q1��Q2�Ĺ�ϵΪ
A��Q1��Q2 B��Q1��Q2 C��Q1��Q2 D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������۵�Ϊ1535�������ڸ�¯������ʱ��������̼���ϸߵ����ĺϽ���1200�����Ҿ��ۻ��ˣ�������Ϊ
A. ���Ĵ���Խ���۵�Խ��
B. �Ͻ���۵����ɷ����ʵ��۵��
C. ��Ϊ�γ�����̼�Ͻ������۵���
D. �ڸ�¯���ۻ��Ĺ����з����˻�ѧ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ȫˮ��ǩ��ӡ����Ҫ�Ŀ����ʳɷ����£���λΪmg��L����Ca 20��K 39��Mg 3��Zn 0.06��F 0.02�ȣ������ Ca��K��Mg��Zn��F��ָ ���� ��
A. ���� B. Ԫ�� C. �������� D. ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com