
实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,以下判断正确的是( )
A.由极性键构成的极性分子
B.由极性键构成的非极性分子
C.由非极性键构成的极性分子
D.BeCl2中Be采取sp2杂化
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要意义.
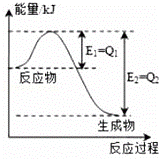
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,如图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式: (△H的数值用含字母Q1、Q2的代数式表示).
(2)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)⇌2SO3(g),混合体系中SO3的体积分数和温度的关系如图1所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题,
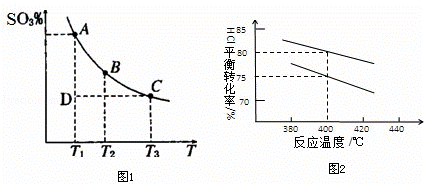
①2SO3⇌2SO2+O2的△H 0.
②若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1 K2;
③反应进行到状态D时,v正 v逆(填<、>或=).
(3)Cl2合成有机物时会产生副产物HC1.4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)可实现氯的循环利用.
①该反应平衡常数的表达式K= ;若反应容器的容积为2L,4min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为 mol/L∙min.
②若该反应在体积不变的密闭容器中发生,当反应达平衡时,下列叙述正确的是 .
a.4v正(HCl)=v逆(O2)
b.又加入1mol O2,达新平衡时,HCl的转化率增大
c.分离出H2O,达新平衡时,v正(HCl)增大
③图2是该反应两种投料比[n (HCl):n (O2)分别为4:1和2:1下,反应温度对HCl平衡转化率影响的曲线.下列叙述正确的是 .
a.其他条件不变,升高温度,平衡常数K值增大
b.若平衡常数K值变大,达新平衡前v逆始终减小
c.若平衡常数K值变大,则平衡向正反应方向移动
④投料比为4:1、温度为400℃时,平衡混合物中
Cl2的物质的量分数是 %.(计算结果保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、101kPa下,稀的强酸与强碱溶液反应的中和热为57.3kJ/mol.
(1)写出表示稀硫酸与稀烧碱溶液发生反应的中和热的热化学方程: .
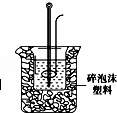
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图.
①实验时所需的玻璃仪器除烧杯、量筒外还需: .
②该装置中有一处错误是: ,如果用该错误
装置测定,结果会 (填“偏高”“偏低”“无影响”)
③如果该生用50mL 0.25mol/L的稀硫酸与50mL 0.55mol/L的稀烧碱溶液,他用试剂的用量的理由是: .在该实验中需要测定某种数据,完成一次实验,需要测定该数据的次数为 次.使用正确的装置进行实验,取上述溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃.已知中和后生成的溶液的比热容为4.18J/(g•℃),溶液的密度均为1g/cm3.通过计算可得中和热△H= .
查看答案和解析>>
科目:高中化学 来源: 题型:
用1.0mol·L-1NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图所示,原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是( )
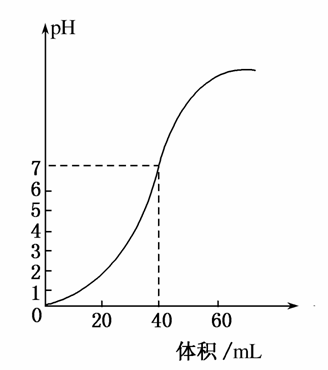
A.1mol·L-1,60mL
B.0.5mol·L-1,80mL
C.0.5mol·L-1,40mL
D.1mol·L-1,80mL
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关σ键的说法错误的是( )
A.如果电子云图象是由两个s电子重叠形成的,即形成ss σ键
B.s电子与p电子可形成sp σ键
C.p电子与p电子不能形成σ键
D.HCl分子里含一个sp σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质两种含氧酸中,前者比后者酸性弱的是( )
A.H2SO4和H2SO3
B.(HO)2RO2和(HO)2RO3
C.HNO3和HNO2
D.H2SiO3和H4SiO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是A、B、C、D、E五种元素的某些性质:
|
| A | B | C | D | E |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是________。
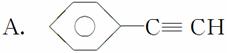
B.CH4
C.CH2===CHCH3
D.CH3CH2C≡CH
E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键___________________________________________。
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是________(化学式),理由是________________________。
(4)B、D形成的氢化物沸点:________更高,热稳定性________更强。(写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 使用食品添加剂与提倡绿色食品相违背 |
|
| B. | 没有食品添加剂的天然食品是最安全的 |
|
| C. | 含有食品添加剂的食品应该少吃,以防中毒 |
|
| D. | 食品添加剂在合理限量范围内不影响人体健康 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com