
【化学—选修5:有机化学基础】(15分)
苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p—xylene,缩写为PX)是化学工业的重要原料。
(1)写出PX的结构简式______________。
(2)PX可能发生的反应有_____ __、___ _____。(填反应类型,只填两种。)
(3)有机物M存在如下图所示的转化关系,其中A 是PX的一种同分异构体。
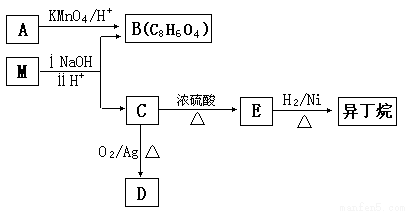
已知:M的分子式为C16H22O4,D能发生银镜反应。
①B的苯环上存在3 种不同化学环境的氢原子,则B 的结构简式是__________。
②D分子中所含的官能团是______________(填化学式)。
③M的结构简式是_______________。
(4)F是B 的一种同分异构体,具有如下特征:
a.是苯的对位二取代物;b.遇FeCl3溶液显示紫色;c.能与碳酸氢钠溶液反应。
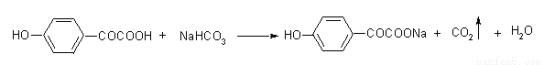
写出F与NaHCO3溶液反应的化学方程式_____________________________。
(15分)
(1) 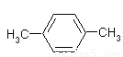 (2分,左侧的H3C写成CH3不扣分)
(2分,左侧的H3C写成CH3不扣分)
(2)取代反应 、加成反应、氧化反应只要两个即可(或其它合理答案)(共2分,各1分)
(3)
① 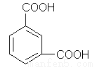 (3分) ② —CHO或
(3分) ② —CHO或 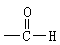 (2分,写名称给1分)
(2分,写名称给1分)
③ 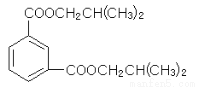 (3分,侧链H原子数错扣1分,其它错误0分)
(3分,侧链H原子数错扣1分,其它错误0分)
(4)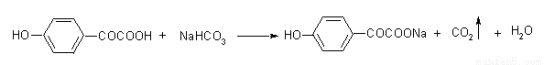
(3分,生成物中CO2、H2O没写扣1分,NaHCO3写在箭头上也可。)
【解析】
试题分析:(1)对二甲苯的结构简式为 
(2)对二甲苯中存在苯环、甲基,所以可以发生加成反应、氧化反应、取代反应;
(3)①A 是PX的一种同分异构体,所以A被氧化得二元羧酸B,只有间苯二甲酸的苯环上有3种氢原子,所以B的结构简式为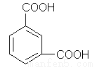
②D能发生银镜反应,说明D中存在醛基,结构简式为—CHO;
③由流程图判断M是酯类,C属于醇且能被氧化为醛,说明C中存在-CH2H结构,C最终能得到异丁烷,所以C是2-甲基-1-丙醇,则M是1分子B与2分子C酯化的产物,结构简式为
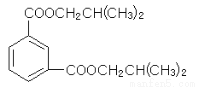
(4)由题意知,F中存在酚羟基和羧基,且只有2个对位取代基,所以F中的取代基是-OH、-COCOOH,则F与碳酸氢钠反应的化学方程式为
考点:考查有机物结构简式、化学方程式的推断与书写,官能团的结构与性质,物质推断,同分异构体的判断


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源:2013-2014河南省周口市高一下学期5月联考化学试卷(解析版) 题型:选择题
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60 ml B.45 ml. C.30 mL D.15mL
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省南阳市春期高一期终质量评估化学试卷(解析版) 题型:选择题
铝土矿的主要成分中含有氧化铝、氧化铁和二氧化硅等,工业上经过下列工艺可以冶炼
金属铝。下列说法不正确的是( )
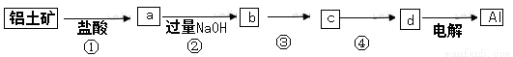
A.①、②中除加试剂外,还需要进行过滤操作
B.a、b中铝元素的化合价相同
C.③中需要通入过量的氨气
D.④进行的操作是加热,而且d一定是氧化铝
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省六市毕业班第二次联合调研检测理综化学试卷(解析版) 题型:填空题
【化学--选修3物质结构与性质】(15分)
铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
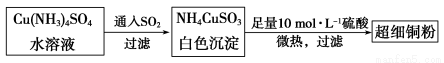
①Cu2+的价电子排布图 ; NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为_______________________(填元素符号)。
②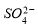 的空间构型为_____________,
的空间构型为_____________,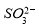 离子中心原子的杂化方式为 。
离子中心原子的杂化方式为 。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式: 。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因 .
(4)Cu晶体的堆积方式如图所示,设Cu原子半径为r,
晶体中Cu原子的配位数为_______,晶体的空间利用率
为 ( 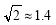 ,列式并计算结果)。
,列式并计算结果)。

查看答案和解析>>
科目:高中化学 来源:2013-2014河南省六市毕业班第二次联合调研检测理综化学试卷(解析版) 题型:选择题
有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱溶液中发生反应的X的同分异构体有(不考虑立体异构)
A.15种 B.13种 C. 11种 D.9种
查看答案和解析>>
科目:高中化学 来源:2013-2014河南师大附中高三4月份月考理综化学试卷(解析版) 题型:简答题
(13分)我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用。
(1)工业上可以用黄铜矿(主要成分CuFeS2)为原料冶炼铜。主要反应如下:
① 2CuFeS2+4O2=Cu2S+3SO2+2FeO ② 2Cu2S + 3O2=2SO2+2Cu2O③ Cu2S+ 2Cu2O=6Cu+ SO2
在③中被氧化与被还原元素原子的物质的量之比为 ;若由3mol CuFeS2生成3molCu,理论上消耗O2 的物质的量为 。
(2)常温下Cu2O能溶于稀硫酸,得到蓝色溶液和红色固体,可以利用该性质检验工业上冶炼铜得到的粗铜中是否含有Cu2O,写出此反应的离子方程式 。
(3)刻蚀印刷电路的废液中含有大量的CuCl2、FeCl2、FeCl3,任意排放将导致环境污染和资源的浪费, 为了使FeCl3循环利用和回收CuCl2,现设计如下生产过程:
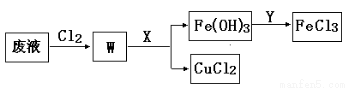
①试剂Y的名称 ;物质X最好是 (填化学式)。
②若常温下1L废液中含CuCl2、FeCl2、FeCl3的物质的量浓度均为0.5 mol· , 则加入Cl2气和物质X使溶液的pH在 范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2 不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38 、 KSP [Cu(OH)2]=2.0×10—20 、 lg5=0.7)
, 则加入Cl2气和物质X使溶液的pH在 范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2 不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38 、 KSP [Cu(OH)2]=2.0×10—20 、 lg5=0.7)
查看答案和解析>>
科目:高中化学 来源:2013-2014河南师大附中高三4月份月考理综化学试卷(解析版) 题型:选择题
化学知识在生产和生活中有着重要的应用,下列说法中不正确的是
A.明矾常做净水剂
B.与铜质水龙头连接处的钢质水管易发生腐蚀
C.发酵粉中含有较多的NaHCO3,能使焙制出的糕点疏松多孔
D.金属钠、金属镁等活泼金属着火时,可以使用泡沫灭火器来灭火
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省邯郸市高二7月调研考试化学试卷(解析版) 题型:选择题
在101 kPa和298 K时,有关反应的热化学方程式有:
H2(g)+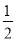 O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
H2(g)+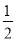 O2(g)===H2O(l) ΔH2=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH2=-285.8 kJ·mol-1
下列说法错误的是( )
A.H2燃烧生成1 mol H2O(g)时,放出241.8 kJ的热量
B.O2前面的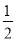 表示参加反应的O2的分子数目
表示参加反应的O2的分子数目
C.燃烧热是以在101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则 H2的燃烧热为285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省高一下学期第三次月考化学试卷(解析版) 题型:填空题
(14分)Ⅰ、某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1) A与溴的四氯化碳溶液反应的化学方程式为 ;
(2)已知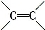
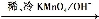
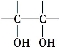
请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得产物与足量乙酸反应的化学方程式 ;
(3)在一定条件下,由A聚合得到的高分子化合物的结构简式为 。
(4) A与氢气完全加成后的一氯代物共有 种。
Ⅱ、用如图所示装置制取乙酸乙酯,请回答以下问题。
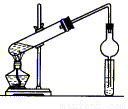
(5)在试管中配制一定比例的乙醇、乙酸和浓H2SO4的混合液的方法是_______
(6)末端干燥管的作用是_______________。
(7)实验结束后,取下盛有饱和碳酸钠溶液的试管,再沿该试管内壁缓缓加入紫色石蕊试液1毫升,发现石蕊层为三层环,由上而下是颜色为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com