
| A. | 0.80g | B. | 0.02g | C. | 0.23g | D. | 0.46g |
分析 钠铝合金置于水中,合金全部溶解,发生2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,加盐酸时可能发生NaOH+HCl═NaCl+H2O、NaAlO2+HCl+H2O═NaCl+Al(OH)3↓、Al(OH)3↓+3HCl═AlCl3+3H2O,结合加入20mL盐酸生成的沉淀最多来计算.
解答 解:由钠铝合金置于水中,合金全部溶解,发生2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,加盐酸时可能发生NaOH+HCl═NaCl+H2O、NaAlO2+HCl+H2O═NaCl+Al(OH)3↓、Al(OH)3↓+3HCl═AlCl3+3H2O可知,
加入1mol/L盐酸20mL,此时沉淀量达到最大值,溶液中的溶质只有NaCl,
则n(Na)=n(NaCl)=n(HCl)=0.02L×1mol/L=0.02mol,其质量为0.02mol×23g/mol=0.46g,
故选D.
点评 本题考查Al的化学性质及计算,为高频考点,题目难度中等,把握发生的反应及原子守恒为解答的关键,注意判断沉淀最多时溶质为NaCl即可解答,侧重分析与计算能力的考查.


科目:高中化学 来源: 题型:选择题
| A. | 选用480 mL 容量瓶 | |
| B. | 把烧碱固体放在纸上称量 | |
| C. | 把称好的固体放入容量瓶中稀释至刻度线 | |
| D. | 定容时俯视容量瓶的刻度线浓度偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
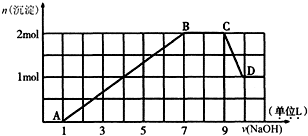
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | A | B |
| 浓度/(mol•L-1) | 0.4 | 0.6 |
| A. | a=1.0 | |
| B. | 此时刻正反应速率小于逆反应速率 | |
| C. | 在相同条件下,若起始时加入2amolA,则达到平衡时A的转化率减小 | |
| D. | 若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
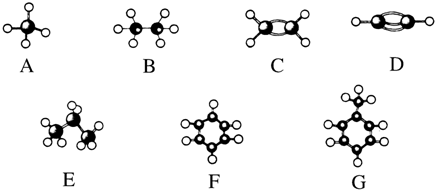
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b>a>c | B. | c>a>b | C. | a>b>c | D. | a=b=c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com