
【题目】高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程:
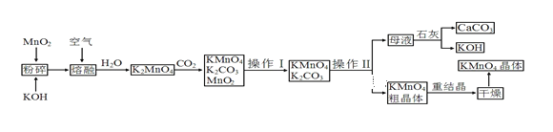
(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列_____物质相似。
A 75%酒精 B 双氧水 C 苯酚 D “84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是________;
(3)上述流程中可以循环使用的物质有石灰、CO2、____,____;(写化学式)。
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是_______。
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:___________。
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:__________。
【答案】BD 过滤 KOH MnO2 K2MnO4 2Mn2++5NaBiO3+14H+=2MnO4+5Bi3++5Na++7H2O 2MnO2+4KOH+O2![]() 2K2MnO4+2H2O
2K2MnO4+2H2O
【解析】
将MnO2和KOH粉碎,目的是增大反应物的接触面积,加快反应速率,然后将混合物熔融并通入空气,根据流程图知,二者反应生成K2MnO4,根据元素守恒知还生成H2O,K2MnO4和CO2反应生成KMnO4、K2CO3、MnO2,KMnO4、K2CO3易溶于水而MnO2难溶于水,将KMnO4、K2CO3、MnO2溶于水然后过滤得到KMnO4、K2CO3混合溶液,再根据KMnO4、K2CO3溶解度差异采用加热浓缩、冷却结晶的方法获得KMnO4晶体,母液中含有K2CO3,加入CaO,发生反应K2CO3+CaO+H2O=CaCO3↓+2KOH,从而得到KOH;将KMnO4晶体洗涤干燥得到纯净的KMnO4晶体。
(1)KMnO4有强氧化性,利用其强氧化性杀菌消毒,消毒原理与双氧水、NaClO一样,故答案为:BD;
(2)K2MnO4和CO2反应生成KMnO4、K2CO3、MnO2,KMnO4、K2CO3易溶于水而MnO2难溶于水,将KMnO4、K2CO3、MnO2溶于水然后过滤得到KMnO4、K2CO3混合溶液,操作Ⅰ的名称是过滤,故答案为:过滤;
(3)制备中利用的原料,在转化过程中又生成的可以循环利用.由转化关系图知,除石灰、二氧化碳外,K2MnO4溶液中通入CO2以制备KMnO4生成的MnO2及最后由母液加入石灰生成的KOH,会在MnO2、KOH的熔融制备K2MnO4中被循环利用,故答案为:KOH;MnO2;
(4)由工艺流程转化关系可知,向K2MnO4溶液中通入CO2制备KMnO4、还生成K2CO3、MnO2,反应只有Mn元素的化合价发生变化,由+6价降低为+4价,由+6价升高为+7价,所以K2MnO4既是氧化剂又是还原剂,故答案为:K2MnO4;
(5)铋酸钠(不溶于水)在酸性溶液中与Mn2+反应生成MnO4-和Bi3+,则反应的离子方程式为:2Mn2++5NaBiO3+14H+=2MnO4+5Bi3++5Na++7H2O;故答案为:2Mn2++5NaBiO3+14H+=2MnO4+5Bi3++5Na++7H2O;
(6)由工艺流程转化关系可知,MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,根据元素守恒还应生成水.反应中锰元素由+4价升高为+6价,总升高2价,氧元素由0价降低为-2价,总共降低4价,化合价升降最小公倍数为4,所以MnO2系数2,O2系数为1,根据锰元素守恒确定K2MnO4系数为2,根据钾元素守恒确定KOH系数为4,根据氢元素守恒确定H2O系数为2,所以反应化学方程式为2MnO2+4KOH+O2![]() 2K2MnO4+2H2O,故答案为: 2MnO2+4KOH+O2
2K2MnO4+2H2O,故答案为: 2MnO2+4KOH+O2![]() 2K2MnO4+2H2O。
2K2MnO4+2H2O。


科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:
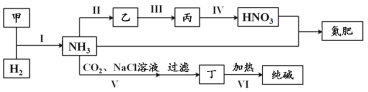
下列说法不正确的是
A.甲、乙、丙三种物质中都含有氮元素
B.反应II、III和Ⅳ的氧化剂相同
C.VI的产物可在上述流程中被再次利用
D.V中发生反应:NH3+CO2+H2O+NaCl===NaHCO3↓+NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.写出下列典型物质的电离方程式
(1)H2SO4_________________________________________
(2)Fe(OH)3________________________________________
(3)NaHSO4_________________________________________
(4)NaHCO3________________________________________
(5)Al2O3(熔融)____________________________________
II.写出下列典型反应的离子方程式:
(1)在稀H2SO4中加入CH3COONa溶液___________________________________
(2)氧化镁溶于稀硫酸______________________________________________
(3)CuSO4溶液与Ba(OH)2溶液混合_______________________________________
(4)NaHCO3溶液与稀盐酸混合________________________________________
(5)NaHSO4溶液与NaOH溶液混合_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向300 mL 1 mol·L-1的稀硝酸中,加入5.6 g铁粉,充分反应后,铁粉全部溶解(假设还原产物只有NO),下列说法不正确的是( )
A. 最终所得溶液中既有Fe2+又有Fe3+
B. 最终溶液中,硝酸无剩余
C. 标准状况下生成NO的体积为1.68 L
D. 再向最终所得溶液中滴加稀硝酸,无明显变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液中只可能大量存在NH4+、Na+、Ag+、Ba2+、MnO4-、Fe3+、CO32-、SO42-、NO3-中的几种离子。从其中取两份各100mL,进行如下实验:
(1)不做任何实验就可以肯定原溶液中不存在的两种离子是__、__。
(2)取其中的一份进行实验,加入过量氢氧化钠溶液并加热,生成气体0.06mol。另取其中的一份加入过量Ba(NO3)2溶液,生成白色沉淀4.30g,过滤,向沉淀中再加入过量稀盐酸,沉淀部分消失,余下沉淀2.33g。综上所述说明原溶液中肯定存在的各离子浓度分别是(下面填写要求:例如c(Na+)=0.1mol/L)__、__、__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化学反应因反应条件不同,可生成不同的有机产品。例如: HX+CH3-CH=CH2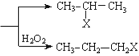 (X为卤素原子),工业上利用上述信息,按下列路线合成结构简式为
(X为卤素原子),工业上利用上述信息,按下列路线合成结构简式为![]() 的物质,该物质是一种香料。
的物质,该物质是一种香料。
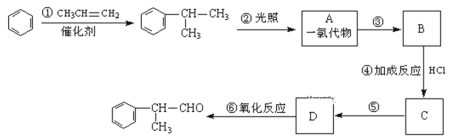
请根据上述路线,回答下列问题:
(1)A的结构简式可能为__________和__________;
(2)反应③、⑤的反应类型分别为________、_______;
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):________;
(4)这种香料具有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色、②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写两种):_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据如图关系推断:
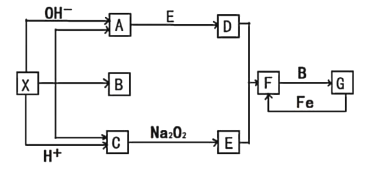
(1)写出化学式:A____,G____。
(2)实验室收集气体D和A的方法依次是____法、_____法。
(3)写出C→E的化学方程式:____。
(4)请写出A与E反应生成D的化学方程式:_____。
(5)检验物质A的方法和现象是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上生产高氯酸时,还同时生产了一种常见的重要合氯消毒剂和漂白剂亚氯酸钠(NaClO2),工艺流程如下:
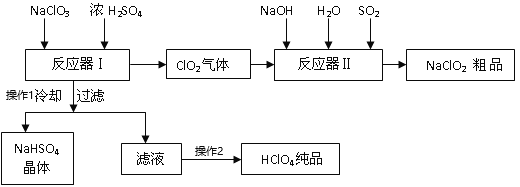
已知:a. NaHSO4的溶解度随着温度的升高而增大,适当条件下可结晶析出;
b.高氯酸是至今为止人们已知酸中的最强酸,沸点:90℃。
(1)操作①冷却过滤的目的是__________________
(2)反应器I中发生化学反应的方程式是_________________,反应器I中的温度最佳为__________(填序号);操作②的名称为______________。
A.0℃ B. 20℃ C. 80℃ D. 120℃
(3)反应器II中发生反应的离子方程式为_________;SO2的作用为_______________(氧化剂、还原剂)。
(4)加快反应器II中反应速率的措施有___________(写出2种措施即可)等。从反应器II中获得NaClO2粗品的实验操作依次是______________(选序号,下同),进一步提纯的操作名称为______________
A.过滤 B.重结晶 C.蒸馏 D.蒸发浓缩 E.蒸干灼烧 F.冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
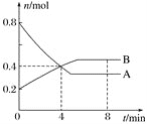
(1)从反应开始至4 min时,A的平均反应速率为___。
(2)该反应的化学方程式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com