
【题目】某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
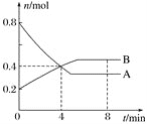
(1)从反应开始至4 min时,A的平均反应速率为___。
(2)该反应的化学方程式为___。
【答案】0.05 mol·L-1·min-1 2A![]() B
B
【解析】
(1)由图可以看出,在4 min末n(A)=0.4mol,Δn(A)=0.8-0.4=0.4mol,从0到4 min内Δc(A)=0.4mol ÷2=0.2mol·L-1, v(A)=![]() 0.05 mol·L-1·min-1。
0.05 mol·L-1·min-1。
(2)根据图像,0到4 min内,A物质的量减少0.4mol,A是反应物,B物质的量增加0.2mol,B是生成物,各物质的物质的量变化之比为n(A)∶n(B)=0.4mol∶0.2mol=2∶1,4 min后的一段时间以后A、B的物质的量不再改变,证明该反应达到化学平衡,此反应为可逆反应,所以反应方程式是2A![]() B。
B。


科目:高中化学 来源: 题型:
【题目】高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程:
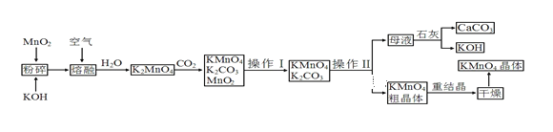
(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列_____物质相似。
A 75%酒精 B 双氧水 C 苯酚 D “84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是________;
(3)上述流程中可以循环使用的物质有石灰、CO2、____,____;(写化学式)。
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是_______。
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:___________。
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有MgCl2和Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的体积关系如图所示,则原溶液中MgCl2和Al2(SO4)3的物质的量浓度之比为( )

A. 1:2 B. 2:1 C. 1:1 D. 2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g)![]() 3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min后达到化学平衡,此时C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1 min-1。
3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min后达到化学平衡,此时C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1 min-1。
(1)5 min末B的物质的量浓度为________。
(2)前5 min内化学反应速率v(A)为_______。
(3)化学方程式中n值为________。
(4)该反应在此温度下的平衡常数K=______(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。已知:CO(g)+H2O(g)![]() H2(g)+CO2(g)的平衡常数随温度的变化如表:
H2(g)+CO2(g)的平衡常数随温度的变化如表:
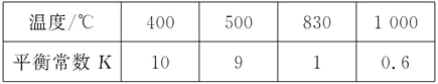
某温度下,平衡浓度符合下式:c(CO2)·c(H2)===c(CO)·c(H2O),试判断此时的温度为__℃。该反应正方向为__(填“放热反应”、“吸热反应”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如下图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
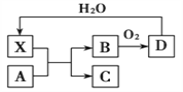
A. X使蔗糖变黑的现象主要体现了X的强氧化性
B. 若A为铁,则足量A与X在室温下即可完全反应
C. 若A为碳单质,则将C通入少量的澄清石灰水,一定可以观察到白色沉淀产生
D. 工业上,B转化为D的反应条件为高温、常压、使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中现用Fe与盐酸反应制取22.4L H2(标准状况下)。
(1)消耗Fe的物质的量为________
(2)如果选用所贴标签为2.0molL-1的盐酸,至少需该盐酸________升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在VL Al2(SO4)3溶液中,含Al3+的质量为a g,则Al2(SO4)3溶液的物质的量浓度为__
(2)有以下物质:①AgCl;②CCl4;③医用酒精;④液氧;⑤二氧化碳;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧食醋;⑨氧化钠固体;⑩氯化氢气体。其中属于电解质的是_____(填序号,下同);属于非电解质的是_____
(3)实验室简单模拟从海水中提取溴单质的部分流程如图
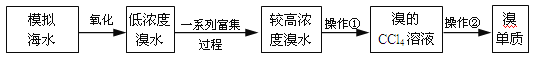
实验操作②的名称_____,操作①中要用到的玻璃仪器_____、_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com