
【题目】实验室中现用Fe与盐酸反应制取22.4L H2(标准状况下)。
(1)消耗Fe的物质的量为________
(2)如果选用所贴标签为2.0molL-1的盐酸,至少需该盐酸________升?
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案科目:高中化学 来源: 题型:
【题目】工业上生产高氯酸时,还同时生产了一种常见的重要合氯消毒剂和漂白剂亚氯酸钠(NaClO2),工艺流程如下:
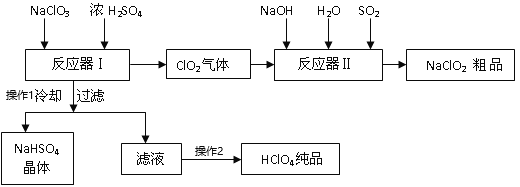
已知:a. NaHSO4的溶解度随着温度的升高而增大,适当条件下可结晶析出;
b.高氯酸是至今为止人们已知酸中的最强酸,沸点:90℃。
(1)操作①冷却过滤的目的是__________________
(2)反应器I中发生化学反应的方程式是_________________,反应器I中的温度最佳为__________(填序号);操作②的名称为______________。
A.0℃ B. 20℃ C. 80℃ D. 120℃
(3)反应器II中发生反应的离子方程式为_________;SO2的作用为_______________(氧化剂、还原剂)。
(4)加快反应器II中反应速率的措施有___________(写出2种措施即可)等。从反应器II中获得NaClO2粗品的实验操作依次是______________(选序号,下同),进一步提纯的操作名称为______________
A.过滤 B.重结晶 C.蒸馏 D.蒸发浓缩 E.蒸干灼烧 F.冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
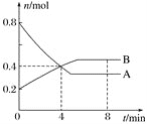
(1)从反应开始至4 min时,A的平均反应速率为___。
(2)该反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器为某些基本操作的部分仪器,请按照要求填空:
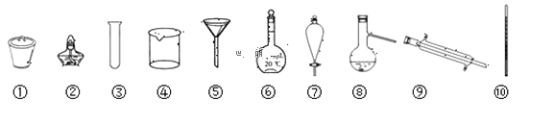
(1)写出仪器的名称:①________;⑦________;⑧________;
(2)上述仪器中,可以直接加热的仪器有________(填序号)。
(3)分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃),需要上述仪器中的(填序号)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯中存在如下平衡:Cl2(g) Cl2(aq)、Cl2(aq)+H2O H++Cl-+HClO。下列说法正确的是( )
A.向饱和氯水中通入HCl,有c(H+)=c(Cl-)+c(OH-)+c(ClO-)
B.向氯水中滴入几滴石蕊试液,溶液变红色
C.光照后的氯水漂白性增强
D.若向饱和氯水中通入少量SO2,则![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置中提供的物质完成相关实验,最合理的选项是( )
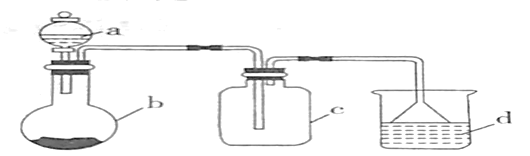
选项 | a中的溶液 | b中的物质 | c中收集的气体 | d中的液体 |
A | 浓氨水 | 生石灰 | NH3 | H2O |
B | 浓硝酸 | 铜片 | NO2 | H2O |
C | 稀硝酸 | 铜片 | NO | NaOH溶液 |
D | 浓硫酸 | 亚硫酸钠 | SO2 | NaOH溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取的工艺流程图如下:
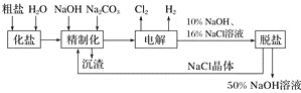
(1)在电解过程中,与电源正极相连的电极上所发生反应的电极反应式为______________,与电源负极相连的电极上所发生反应的电极反应式为__________________。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程中发生反应的离子方程式为________________________________________________________________________。
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是______(填字母)。
,该钡试剂可以是______(填字母)。
a、Ba(OH)2 b、Ba(NO3)2 c、BaCl2
(4)为有效除去Ca2+、Mg2+、![]() ,加入试剂的合理顺序为________。
,加入试剂的合理顺序为________。
a、先加NaOH,后加Na2CO3,再加钡试剂
b、先加NaOH,后加钡试剂,再加Na2CO3
c、先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、结晶、________(填写操作名称)除去NaCl。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,稀释0.1 mol·L-1Na2CO3溶液,图中的纵坐标可以表示
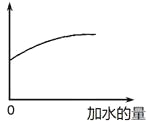
A. CO32-水解的平衡常数
B. 溶液的pH
C. 溶液中HCO3-的数目
D. 溶液中的c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯、硫、氮元素广泛存在于自然界中,对人类生命和生活具有重要意义。
(1)氯气的颜色____________________。
(2)浓硫酸具有:①酸性,②强氧化性,③吸水性,④脱水性,下列各现象硫酸所表现出的性质为(填序号):
干燥氯气 ___________ ,使蔗糖变黑 ___________,
吸收氨气 ___________ ,与铜反应____________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com