
��-���Ȼ�ѧѭ������ʾ��ͼ���£�

��1����Ӧ1�����ӷ���ʽΪ ��
��2����Ӧ2����ת����Ҫ��ʽΪ ��
��3����Ӧ3�п��Ʒ�Ӧ��������Ҫ����ͬ����������立ֽ���ﲻͬ������400��ʱ�ֽ⣬�����ˮ������� A��B��C�������壬A�ǿ����к������ĵ��ʣ�B��ʹʪ��ĺ�ɫʯ����ֽ������C��ʹƷ����Һ��ɫ����
A��B��C�������壬A�ǿ����к������ĵ��ʣ�B��ʹʪ��ĺ�ɫʯ����ֽ������C��ʹƷ����Һ��ɫ���� 400��ʱ����立ֽ�Ļ�ѧ����ʽΪ ��
400��ʱ����立ֽ�Ļ�ѧ����ʽΪ ��
��4����Ӧ4����(a)��(b)������Ӧ��ɣ�
H2SO4(l) =SO3(g) +H2O(g),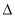 H=+177kJ•mol��1����(a)
H=+177kJ•mol��1����(a)
2SO3(g) 2SO2(g) + O2(g)��
2SO2(g) + O2(g)��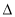 H=+196 kJ•mol��1����(b)
H=+196 kJ•mol��1����(b)
����H2SO4(l)�ֽ�ΪSO2(g)��O2(g)��H2O(g)���Ȼ�ѧ����ʽΪ�� ��
���ں����ܱ������У����Ʋ�ͬ�¶Ƚ���SO3�ֽ�ʵ�顣��SO3��ʼŨ�Ⱦ�Ϊcmol��L��1���ⶨSO3��ת���ʣ������ͼ��ͼ�Т�����ΪSO3��ƽ��ת�������¶ȵĹ�ϵ�������߱�ʾ��ͬ�¶��·�Ӧ������ͬ��Ӧʱ����δ�ﵽ��ѧƽ��ʱSO3��ת���ʡ�
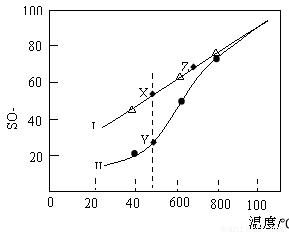
i��ͼ�е�X���Z��ƽ�ⳣ��K��K(X) K(Z)��ѡ���������������
ii��Y���Ӧ�¶��µķ�Ӧ���ʣ�v(��) v(��)��ѡ���������������
iii�����¶ȵ����ߣ������߱ƽ������ߵ�ԭ���ǣ� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ��һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�����������˵������ȷ����
A��H2SO4��Ħ��������g/mol����NA��������ӵ�����(g)����ֵ�����
B��NA���������Ӻ�NA���������ӵ�������Ϊ8��7
C��1mol��L-1 CaCl2��Һ������Ca2+���ӵ���ĿΪNA
D��1mol D2��������ӣ��к���2NA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���ӦaX(g) bY(g) + cZ(g) �ﵽƽ��״̬�����������ѹ����ԭ����1��2���Ҵﵽ�µ�ƽ��״̬ʱ��X�����ʵ���Ũ�ȴ�0.1mol��L����0.19mol��L�������ж���ȷ����
bY(g) + cZ(g) �ﵽƽ��״̬�����������ѹ����ԭ����1��2���Ҵﵽ�µ�ƽ��״̬ʱ��X�����ʵ���Ũ�ȴ�0.1mol��L����0.19mol��L�������ж���ȷ����
A��a��b+c B��a��b+c C��a=b+c D��a=b=c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���У�����ȷ����
A����ѧ��һ�ž��м�ǿʵ���ԵĿ�ѧ
B����ѧʵ���ܽ����ѧѧ�Ƶ���������
C���о����ʵ����ʳ����ù۲졢ʵ�顢���ࡢ�Ƚϵȷ���
D��Ӣ����ѧ�ҵ��������ԭ��ѧ˵��Ϊ������ѧ�ķ�չ�춨�˼�ʵ�Ļ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ�ĵ���У������ѧ�ڵڶ���������ѧ�Ծ��������棩 ���ͣ�ѡ����
a mol FeS��b mol FeOͶ�뵽V L c mol��L-1��������Һ�У�ǡ����ȫ��Ӧ����ԭ����ֻ��NO�����ó����� Һ�ɿ�����Fe(NO3)
Һ�ɿ�����Fe(NO3) 3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
�٣�a+b����63g
�ڣ�a+b����189g
�ۣ�a+b��mol
�ܣ�Vc-3a-b/3��mol
A���ڢ� B���ڢ� C���٢� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�γ��и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ֵĿ�����Աȷ�ϻ��ǵر��������и������ε�Һ̬ˮ�������й�ˮ���������ε�˵���������
A��ˮ��һ���������
B��NH4ClO4��Һ������
C��NaClO4�к������Ӽ����ۼ�
D��NH4ClO4ֻ�������ԣ�û�л�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�˲��и߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ʵ���Ҳ��1mol SO2�������л�ѧ��Ӧ��2SO2(g��+O2(g�� 2SO3(g�� ��H����196 kJ/mol�����ų�49kJ����ʱ��SO2ת������ӽ���
2SO3(g�� ��H����196 kJ/mol�����ų�49kJ����ʱ��SO2ת������ӽ���
A��40% B��50% C��80% D��90%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�����и�һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ��Ӧ�������ӷ���ʽH+ ʮOH- =H2O����ʾ����
A�������������ͭ B�����������������Һ
C�����������������Һ D��ϡ����Ͱ�ˮ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ����11���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
���Ӻͱ�ͪ������Ҫ�Ļ���ԭ�ϣ���ҵ�Ͽ���������������������Ӻͱ�ͪ���䷴Ӧ��������ʾ��ͼ���£�
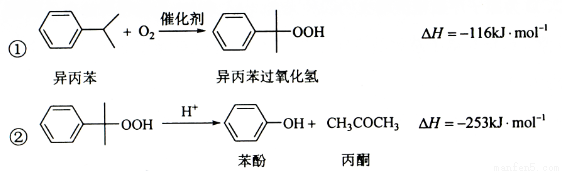
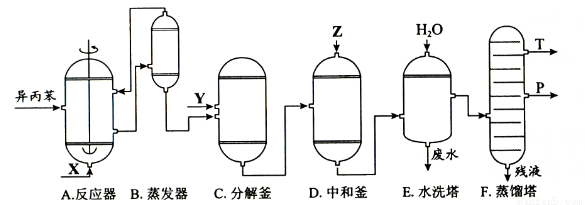
��ػ��������������
���� | ��Է������� | �ܶȣ�g/cm-3�� | �е�/�� |
����� | 120 | 0.8640 | 153 |
��ͪ | 58 | 0.7898 | 56.5 |
���� | 94 | 1.0722 | 182 |
�ش��������⣺
��1���ڷ�Ӧ��A��ͨ���X�� ��
��2����Ӧ�ٺ͢ڷֱ���װ�� �� �н��У���װ�÷��ţ���
��3���ڷֽ⸪C�м����YΪ����Ũ���ᣬ��������______���ŵ��������٣�ȱ����_____��
��4����Ӧ��Ϊ (����ȡ������ȡ�����Ӧ����Ӧ�¶ȿ�����50-60�棬�¶ȹ��ߵİ�ȫ���� �� ��
��5���к�D�м����Z�����˵���  �����š���֪������һ�����ᣩ
�����š���֪������һ�����ᣩ
A�� NaOH B�� CaCO C�� NaHCO D�� Ca O
O
��6��������F�е������T��P�ֱ�Ϊ �� ���жϵ������� ��
��7���ø÷����ϳɱ��Ӻͱ�ͪ���ŵ��� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com