
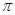 键有___________mol。
键有___________mol。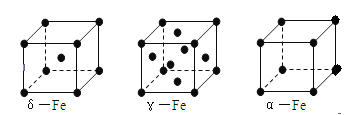
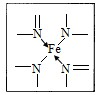 (3)> (4)3
(3)> (4)3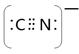 ;2NA (6)4;4:3
;2NA (6)4;4:3 。
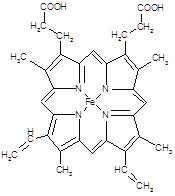
。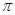 键,因此反应中形成的
键,因此反应中形成的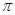 键有1.5mol×2=3mol。
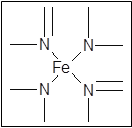
键有1.5mol×2=3mol。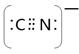 ;O22+与氮气也互为等电子体,则1 mol O22+中含有的π键数目为2NA。
;O22+与氮气也互为等电子体,则1 mol O22+中含有的π键数目为2NA。 +6×
+6× =4,δ、α两种晶胞中铁原子的配位数分别为8、6,则配位数之比为8:6=4:3。
=4,δ、α两种晶胞中铁原子的配位数分别为8、6,则配位数之比为8:6=4:3。

 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源:不详 题型:单选题
| A.每一周期元素都是从碱金属开始,以稀有气体结束 |
| B.f区都是副族元素,s区和p区的都是主族元素 |
| C.已知在20℃1molNa失去1mol电子需吸收650kJ能量,则其第一电离能为650KJ/mol |
| D.Ge的电负性为1.8,则其是典型的非金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径大小:Na>S>O |
| B.金属性强弱:K>Na>Ca |
| C.酸性强弱:HIO4>HBrO4>HClO4 |
| D.碱性强弱:LiOH>NaOH>KOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
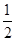 。下列说法正确的是
。下列说法正确的是| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线形共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由Y、Z、M三种元素形成的化合物中只含有共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
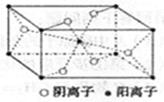
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
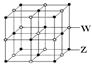
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
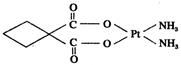
| A.极性共价键 | B.非极性共价键 | C.配位键 | D.离子键 |
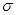 键 G.
键 G.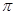 键
键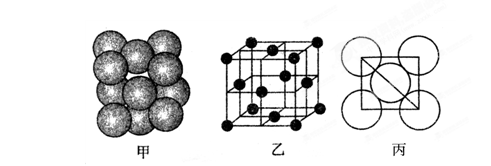
 = g/cm3。(用含M、NA、b的计算式表示,不用化简)。
= g/cm3。(用含M、NA、b的计算式表示,不用化简)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
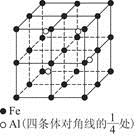
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
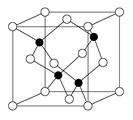
| A.砷化镓晶胞结构与NaCl相同 |
| B.GaP与GaAs互为等电子体 |
| C.电负性:As>Ga |
| D.砷化镓晶体中含有配位键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com