
下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入
前者,反应现象相同的是
A.FeSO4和酸性KMnO4 B.AlCl3和NaOH
C.Na2CO3和HCl D.Ca(HCO3)2和NaOH
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是
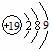 A.钾原子结构示意图: B.间羟基苯甲酸的结构简式:
A.钾原子结构示意图: B.间羟基苯甲酸的结构简式:
|
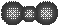
 D.Na2S的电子式:
D.Na2S的电子式: 查看答案和解析>>
科目:高中化学 来源: 题型:
哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2 2NH3 。下列有关说法正确的是:
2NH3 。下列有关说法正确的是:
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
C.达到化学平衡时,反应则停止进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—选修3 物体结构与性质】(15分)
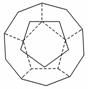 I.德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如右图。
I.德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如右图。
①C20分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②多面体的顶点数、面数和棱边数的关系,遵循欧拉定理 :,顶点数+面数+棱边数=2,
请回答: C20分子共有________个正五边形,共有________条棱边。
II.A、B、C是短周期非金属元素,核电荷数依次增大。A原子外围电子排布为ns2np2,C是地壳中含量最多的元素。D元素的核电荷数为29。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为________。
(2)分子(AB)2中键与键之间的夹角为180°,并有对称性,每个原子最外层电子数均满足八电子,其结构式为________,1 mol该分子中含有π键的数目为________。该分子中碳原子的杂化轨道类型是__________________,该分子属于________分子(填“极性”或“非极性”)。
(3)基态D原子的电子排布式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各种溶液中,能大量共存的无色透明的离子组
A.PH=0的溶液:CH3COO- 、NO3-、SO42-、I-
B.C(H+)=10-14mol/L的溶液中:Na+ 、AlO2-、S2-、SO32-
C.酸性环境下:Na+、Cu2+、NO3-、SO42-、
D.pH=7的溶液中:K+ 、Na+ 、Fe3+ 、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶
 液,溶液中pOH [ pOH=-lg(OH—) ]与pH的变化
液,溶液中pOH [ pOH=-lg(OH—) ]与pH的变化
关系如图所示,则下列说法正确的是
A.M点所示溶液导电能力强于Q点
B.M点和N点所示溶液中水的电离程度相同
C. N点所示溶液中c(CH3COO-)>c(Na+)
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,碳钢腐蚀与溶液pH的关系如下:
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蚀快慢 | 较快 | 慢 | 较快 | ||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2— |
下列说法不正确的是
A.在pH<4溶液中,碳钢主要发生析氢腐蚀
B.在pH>6溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e—=2H2O
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在含CH3COOH和CH3COONa均为0.1mol/L的溶液中,测得pH<7,则下列说法中正确的是
A.c(CH3COO-)<c(Na+) B. c(CH3COOH) + c(CH3COO-)=0.2mol/L
C.c(CH3COOH) > c(CH3COO-) D.c(CH3COO-)>c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是 ( )。
A.标准状况下,2.24 L Cl2通入足量NaOH溶液中,反应转移电子的数目为
0.2NA
B.常温下,0.1 mol·L-1 NH4NO3溶液中NO3-数目为0.1NA
C.常温常压下,4.0 g CH4中含有共价键的数目为NA
D.标准状况下,22.4 L CHCl3含有分子的数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com