
一定温度下,在固定容积的密闭容器中,可逆反应:mA(g)+nB(g)  pC(g)+qD(g),当m、n、p、q为任意正整数时,下列状态:
pC(g)+qD(g),当m、n、p、q为任意正整数时,下列状态:
①体系的压强不再发生变化;
②生成m mol A 同时消耗q mol D;
③各组分的物质的量浓度不再改变;
④体系的密度不再发生变化;
⑤反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q;
⑥各组分的质量分数不再改变;
⑦反应混合物中各物质的物质的量之比为m∶n∶p∶q。
其中一定能说明反应已达到平衡状态的是( )
A.③④⑦ B.①③④⑤ C.②③⑤⑥ D.③⑥
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
(一) 尿素又称碳酰胺,是含氮量最高的氮肥,工业上利用二氧化碳和氨气在一定条件下合成尿素。其反应分为如下两步:
第一步:2NH3(l)+CO2(g) 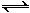 H2NCOONH4(氨基甲酸铵) (l) △H1= —330.0 kJ·mol-1
H2NCOONH4(氨基甲酸铵) (l) △H1= —330.0 kJ·mol-1
第二步:H2NCOONH4(l) 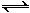 H2O(l)+H2NCONH2(l) △H2= + 226.3 kJ·mol-1
H2O(l)+H2NCONH2(l) △H2= + 226.3 kJ·mol-1
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 m3 密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:
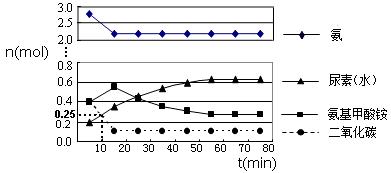
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定。
②反应进行到10 min时测得CO2的物质的量如上图所示,则用CO2表示的第一步反应的速率v(CO2)= mol/(L·min)。
③当反应在一定条件下达到平衡,若在恒温、恒容下再充入一定量气体He,则CO(NH2)2(l)的质量_________(填“增加”、“减小”或“不变”)。
(二)氨是制备尿素的原料,NH3、N2H4等在工农业生产、航空航天等领域有广泛应用。
氨气溶于水得到氨水,在25℃下,将amol/L的氨水与bmol/L的硫酸以3∶2体积比混合反应后溶液呈中性。用含a和b的代数式表示出氨水的电离平衡常数为_________。
(三)氢气是合成氨的原料。“氢能”将是未来最理想的新能源。
(1)在25℃,101KPa条件下,1 g氢气完全燃烧生成液态水时放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为 。
(2)氢气通常用生产水煤气的方法制得。其中C(s)+ H2O(g)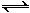 CO(g)+H2(g),在850℃时平衡常数K=1。若向1升的恒定密闭真空容器中同时加入x mol C和6.0mol H2O。
CO(g)+H2(g),在850℃时平衡常数K=1。若向1升的恒定密闭真空容器中同时加入x mol C和6.0mol H2O。
①当加热到850℃反应达到平衡的标志有______________ 。
A.容器内的压强不变 B.消耗水蒸气的物质的量与生成CO的物质的量相等
C.混合气的密度不变 D.单位时间有n个H-O键断裂的同时有n个H-H键断裂
②x应满足的条件是 。
(四)CO2是合成尿素的原料,但水泥厂生产时却排放出大量的CO2。华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示:
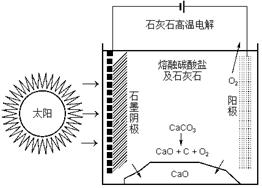
(1)上述生产过程的能量转化方式是 。
(2)上述电解反应在温度小于900℃时进行碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为 ,阴极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。已知空气的平均相对分质量为29,则A的相对分子质量是 ( )
A. 29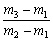 B.29
B.29
C. 29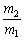 D.29
D.29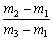
查看答案和解析>>
科目:高中化学 来源: 题型:
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)卤族元素位于周期表的_________区;溴的电子排布式为______________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在。使氢氟酸分子缔合的作用力是 。
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 。
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |

(4)已知高碘酸有两种形式,化学式分别为H5IO6和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4(填“>”、“<”或“=”)
(5)已知ClO2-立体构型为V型。ClO2-中心氯原子的杂化轨道类型为___________,写出CN-的等电子体的化学式__________(写出1个)
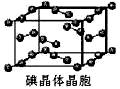 (6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
(6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
A、用均摊法可知平均每个晶胞中有4个碘原子
B、碘晶体为无限延伸的空间结构,是原子晶体
C、碘晶体中存在非极性键和范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
对反应A+3B 2C来说,下列反应速率中最快的是( )
2C来说,下列反应速率中最快的是( )
A.v(A)=0.3 mol/(L·min) B.v(B)=0.6 mol/(L·min)
C.v(C)=0.5 mol/(L·min) D.v(A)=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断不合理的是( )
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断不合理的是( )
A.c1∶c2=1∶3 B.平衡时,Y和Z的生成速率之比为3∶2
C.X、Y的转化率不相等 D.c1的取值范围为0<c1<0.14 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中正确的是 
























 ( ) A.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
( ) A.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
B.Ba(NO3)2 溶于水,可将含Ba(NO3)2 的废液倒入水槽中,再用水冲入下水道
C. 不慎将浓碱溶液溅到皮肤上,要立即用大量水冲洗,然后再涂硫酸溶液中和
D. 酒精灯不慎着火,应立即用水灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
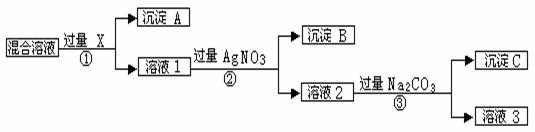
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
请回答下列问题:
⑴写出实验流程中下列物质的化学式: 试剂X : ,沉淀A: ,沉淀B: 。
⑵上述实验流程中加入过量的Na2CO3的目的是 。
⑶按此实验方案得到的溶液3中肯定含有 (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的 ,之后若要获得固体NaNO3需进行的实验操作是 _________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g/mL),所得溶液的密度为ρ g/mL,质量分数为w,物质浓度为c mol/L,则下列关系中不正确的是 ( )
A. ρ=(17V+22 400)/(22.4+22.4V)
B. w=17c/(1 000ρ)
C. w=17V/(17V+22 400)
D.c=1 000Vρ/(17V+22 400)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com