
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)卤族元素位于周期表的_________区;溴的电子排布式为______________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在。使氢氟酸分子缔合的作用力是 。
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 。
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |

(4)已知高碘酸有两种形式,化学式分别为H5IO6和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4(填“>”、“<”或“=”)
(5)已知ClO2-立体构型为V型。ClO2-中心氯原子的杂化轨道类型为___________,写出CN-的等电子体的化学式__________(写出1个)
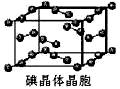 (6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
(6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
A、用均摊法可知平均每个晶胞中有4个碘原子
B、碘晶体为无限延伸的空间结构,是原子晶体
C、碘晶体中存在非极性键和范德华力
科目:高中化学 来源: 题型:
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。请完成下 列空白:
(1)铝元素在周期表中的位置为________。
(2)在19世纪时,铝是一种珍贵的金属。人们最初得到的铝粒如同珍宝,它的价格同黄金 相当。1827年,德国化学家维勒用金属钾与无水氯化铝反应而制得了金属铝。用钾与无水氯化铝反应制铝而不用氯化铝溶液的理由是_________。
现代工业炼铝的原料是由铝土矿提取而得,在提取过程中通入的气体为____。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高 温下煅烧,所得物质可作耐高温材料,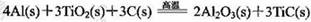
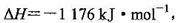 则反应过程中,每转移1 mol电子放出的热量为________。
则反应过程中,每转移1 mol电子放出的热量为________。
(4)硅与铝同周期,地壳里硅铝的含量:硅________铝(填>,<或=)。是硅酸盐玻璃 (Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成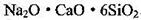 。盛放NaOH溶 液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 ________。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为________。
。盛放NaOH溶 液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 ________。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为________。
(5)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如: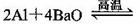
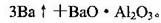 利用化学平衡移动原理解释上述方法可制取金属Ba的原因是
利用化学平衡移动原理解释上述方法可制取金属Ba的原因是
_____________________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2CO3俗名纯碱,下面是对纯碱采用不同的分类,不正确的是 ( )
A.Na2CO3是碱 B.Na2CO3是盐
C.Na2CO3是钠盐 D.Na2CO3是碳酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的离子方程式。
①稀硫酸与NaOH溶液反应的离子方程式:
________________________________________________________________________
②足量稀硝酸与CaCO3溶液反应的离子方程式:
________________________________________________________________________
③锌与稀硫酸反应的离子方程式:
________________________________________________________________________
④稀硫酸和氢氧化钡溶液反应的离子方程式:
⑤等体积等物质的量浓度的碳酸氢钠溶液和氢氧化钡溶液反应的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2的资利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应(未配平):
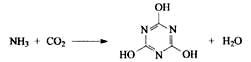
下列有关三聚氰酸的说法正确的是
A、分子式为C3H6N3O3 B、分子中既含极性键,又含非极性键
C、属于共价化合物 D、生成该物质的上述反应为中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.增大反应物浓度,可增大单位体积内活化分子的百分数,使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在固定容积的密闭容器中,可逆反应:mA(g)+nB(g)  pC(g)+qD(g),当m、n、p、q为任意正整数时,下列状态:
pC(g)+qD(g),当m、n、p、q为任意正整数时,下列状态:
①体系的压强不再发生变化;
②生成m mol A 同时消耗q mol D;
③各组分的物质的量浓度不再改变;
④体系的密度不再发生变化;
⑤反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q;
⑥各组分的质量分数不再改变;
⑦反应混合物中各物质的物质的量之比为m∶n∶p∶q。
其中一定能说明反应已达到平衡状态的是( )
A.③④⑦ B.①③④⑤ C.②③⑤⑥ D.③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
使等体积的AlCl3.CaCl2.NaCl溶液中的Cl-完全转化为AgCl沉淀,所用0.1 mol/L AgNO3溶液的体积相同,则这三种溶液的物质的量浓度之比为( )
A.1:2:3 B.1:1:1 C.2:3:6 D.6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A. 在标准状况下,1mol水的体积是22.4L
B. 1molH2所占的体积一定是22.4L
C. 在标准状况下,NA个任何分子所占的体积约为22.4L
D. 在标准状况下,总质量为28g N2和CO的混合气体,其体积约为22.4L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com