
����Ŀ����NAΪ�����ӵ���������ֵ������˵���������

A. 256gS8����(��ͼ)�к�S-S��Ϊ7NA��
B. 1molNa��O2��ȫ��Ӧ������Na2O��Na2O2�Ļ���ת�Ƶ�������ΪNA��
C. ��1molCH3COONa������CH3COOH�γɵ�������Һ�У�CH3COO-��ĿΪNA��
D. һ�������£�2mo1SO2��1molO2������ܱ������г�ַ�Ӧ�������еķ���������2NA
���𰸡�A
��������A. 256gS8�����ʵ���Ϊ1mol��ÿ����������8��S-S������������к�S-S��Ϊ8NA����A����ȷ��B. 1molNa��O2��ȫ��Ӧ������Na2O��Na2O2�Ļ����ƵĻ��ϼ���0���ߵ�+1����ת�Ƶ�������ΪNA����B��ȷ��C. ��1molCH3COONa������CH3COOH�γɵ�������Һ�У������ӵ�Ũ�������������ӵ�Ũ����ͬ���ɵ���غ��֪��CH3COO-��Ŀ����������ͬ������ĿΪNA����D. SO2��O2�ķ�Ӧ�ǿ��淴Ӧ��һ�������£�2mo1SO2��1molO2������ܱ������г�ַ�Ӧ�������еķ���������2NA��D��ȷ������ѡA��


 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д� Сѧ�������Ծ�ϵ�д�
Сѧ�������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ӽ���ķ�����ȷ����
A. ij��Һ![]() �а�ɫ������˵��ԭ��Һ����Cl��
�а�ɫ������˵��ԭ��Һ����Cl��
B. ij��Һ![]() �а�ɫ������˵��ԭ��Һ����SO42��
�а�ɫ������˵��ԭ��Һ����SO42��
C. ij��Һ![]() ����ɫ������˵��ԭ��Һ����Cu2+
����ɫ������˵��ԭ��Һ����Cu2+
D. ij��Һ![]() ������ɫ���壬˵��ԭ��Һ����CO32��
������ɫ���壬˵��ԭ��Һ����CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 0.1mol/LpHΪ4��NaHB��Һ�У�c (HB-)>c(H2B)>c(B2-)
B. ��ͼ��ʾ25��ʱ����0.1mol��L-1����ζ�20mL0.1mol��L-1NaOH��Һʱ����Һ��pH�����������ı仯

C. ��pH=2��NaHSO4��Һ��c(H+)=c(OH-)+ c(SO42-)
D. pH=2������һԪ��x��y�������Ϊ100 mL��ϡ������pH����Һ����Ĺ�ϵ��ͼ��ʾ���ֱ�μ�NaOH��Һ(c=0.1mol��L-1)��pH=3������NaOH��Һ�����ΪVx��Vy����xΪǿ�ᣬyΪ������Vx>Vy

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ������������⣺
��1�����ĵ���ʽ_________________��
��2��д��4-��-2-�һ�-1-��ϩ�ļ���ʽ___________________________��
��3���л���![]() ϵͳ������_______________�������ڴ�����������ȫ�⻯������������ϵͳ������___________________��
ϵͳ������_______________�������ڴ�����������ȫ�⻯������������ϵͳ������___________________��
��4���ٵ����ʵ�����A.�״���B.�Ҵ���C.�Ҷ�����D.���������ֱ�������Ľ��������ã��ų������������ٵ����˳����_______________��
�ڵ�������A.�״���B.�Ҵ���C.�Ҷ�����D.���������ֱ�������Ľ��������ã��ų������������ٵ����˳����_______________��
��ʾ���״���CH3OH���Ҷ�����![]() ����������
����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᴿ�ǻ�ѧʵ���е���Ҫ���֣������й��ˡ���������ȡ������ȣ�Ӧ�ù㷺���������м���Ũ������ʵ�������ˮ �� �� �� �� ��ϩ�ij��� ���� �� ʵ�� �Һϳɻ���ϩ�ķ�Ӧ�� ʵ�� װ ����ͼ��
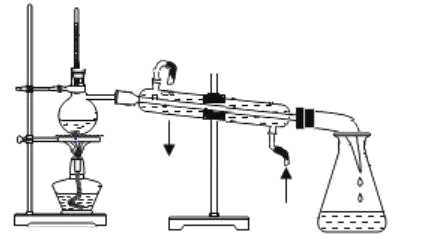
�����õ����й��������£�
��Է������� | �ܶ� / �� gcm�D 3 �� | �е�/�� | �ܽ��� | |
������ | 100 | 0.9618 | 161 | ����ˮ |
�� ��ϩ | 82 | 0.8102 | 83 | ������ˮ |
I.�ϳɷ�Ӧ��
�� a �� ���� 20g ������ �� 2 СƬ���Ƭ����ȴ�������������� 1 ml Ũ �� �� �� b �� ͨ���� ȴˮ��ʼ�������� a �������������¶Ȳ����� 90�森
�� �����ᴿ ��
��Ӧ�ֲ��ﵹ���Һ©�� �� �ֱ������� 5% ̼������Һ��ˮϴ�ӣ� ���� �������ˮ�Ȼ� �ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�����ͨ�� ���� �õ����� �� ��ϩ 10g �� �ش��������⣺
��1���������Ƭ�������� _____�� �� �� �� �� һ �� ʱ �� �� �� �� �� �� �� �� Ƭ �� Ӧ �� �� ȡ ����ȷ������ _____���� ��ĸ���� ����
A ���������� B ����ȴ��
C �����貹�� D ����������
��2���ڱ� ʵ����� ������ ������Ӧ�ôӷ�Һ©���� _______���� ���Ͽڵ��� ���� ���¿ڵ� �� ������ ������ _____��
��3�������ᴿ�� �� �� ������ˮ�Ȼ��Ƶ�Ŀ���� _____��
��4���� �� ��ϩ�ֲ��� ���� ���� �� ���������õ��������� ________���� ��ĸ���� ����
A �� ���� ��ƿ B ���¶ȼ� C ����Һ©��
D ��ţ�ǹ� E ����ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��Fe(OH)2��Cu(OH)2�ı�����Һ�У����������ӵ����ʵ���Ũ�ȵĸ�����[-lgc(M2+)]����ҺpH�ı仯��ϵ��ͼ��ʾ����֪���¶���Ksp[Cu(OH)2]<Ksp[Fe(OH)2]������˵����ȷ����

A. ����a��ʾFe(OH)2������Һ�еı仯��ϵ
B. ��ȥCuSO4��Һ�к��е�����Fe2+���ɼ�����CuO
C. ��Fe(OH)2��Cu(OH)2��������ʱ����Һ��c(Fe2+)��c(Cu2+)=104.6 ��1
D. ��X���Ӧ�ı�����Һ�м�������NaOH���壬��ת��ΪY���Ӧ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ���Ũ����ͬ��NaCl��MgCl2��AlCl3������Һ������Cl���ĸ������ʱ����������Һ�������Ӧ�ǣ�������
A. 1��1��1 B. 1��2��3 C. 3��2��1 D. 6��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����εĻ�ѧʽ��д�����������ʽ�������ƣ�Na2SiO3�� �� ��ʯ[Mg3��Si4O10����OH��2] ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ����Ũ�ȹ�ϵһ����ȷ����
A. 0.1molLNa2CO3��Һ����ˮϡ�ͣ�c(HCO3-)/c(CO32-)��С
B. pH=7�İ�ˮ���Ȼ����Ļ����Һ��:c(Cl-)>c(NH4+)
C. 0.1molL����������Һ��:c(SO42-)>c(Al3+)>c(H+)>c(OH-)
D. pH=2�Ĵ�����Һ��pH=12��NaOH��Һ��������:c(Na+)=c(CH3COO-)+c(CH3COOH)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com