
����ʵ�鲻�ܴﵽԤ��ʵ��Ŀ�ĵ���
| ѡ�� | ʵ������ | ʵ��Ŀ�� |
| A | ��2.5 g CuSO4��5H2O�ܽ���97.5 g ˮ�� | ������������Ϊ1.6%��CuSO4��Һ |
| B | ��ʢ��1 mL��������Һ���Թ��еμ�NaCl��Һ���������г������ɣ��������еμ�Na2S��Һ | ˵��һ�ֳ�����ת��Ϊ��һ���ܽ�ȸ�С�ij��� |
| C | ȡ���������������ˮ�У��μ�����Ba(OH)2��Һ���۲��Ƿ��а�ɫ�������� | ����NaHCO3�������Ƿ�Na2CO3 |
| D | ȡ����Һ©����������ϲ�Һ�� | �²�Һ��ӷ�Һ©���¶˹ܿڷų����رջ�������һ�������������ϲ�Һ��ӷ�Һ©���Ͽڵ��� |
��֪ʶ�㡿��ѧ����ʵ�� J2
���𰸽�����C ������C��Na2CO3����Ba(OH)2��Һ������Ӧ����BaCO3������NaHCO3Ҳ����Ba(OH)2��Һ������Ӧ����BaCO3�������ʲ�����Ba(OH)2��Һ����NaHCO3�������Ƿ�Na2CO3��������BaCl2��Һ���飬�ʴ���
��˼·�㲦�����⿼�����ڻ�ѧʵ���л�����������Һ�����á���Һ�IJ��������ڴ�������������ķ����ڽ������ʵļ�����ע�����ʵ����ʵ��������ϵ�DZ���Ĺؼ��������״����⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2013��2�³��ʽ����˵����κ����飬����������ļ����ע��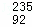 U��һ����Ҫ�ĺ�ȼ�ϣ�����ġ�235����ָ��ԭ�ӵģ�������
U��һ����Ҫ�ĺ�ȼ�ϣ�����ġ�235����ָ��ԭ�ӵģ�������
| �� | A�� | ������ | B�� | ������ | C�� | ������ | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʽÿ��2�֣�����ÿ��1�֣�����8��)
д�����з�Ӧ�Ļ�ѧ����ʽ�����ʵĵ��뷽��ʽ��
��1��д��CO2������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ
��CO2���� ����������Ի���ԣ�
��2��д��Na2O�����ᷴӦ�Ļ�ѧ����ʽ
��Na2O���� ����������Ի���ԣ�
��3��Fe2(SO4)3���뷽��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�㶨�������г���2molA��lmolB������Ӧ��2A(g)+B(g) 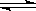 xC(g)�ﵽƽ�� ��C���������Ϊ��������ά���������ݻ����¶Ȳ��䣬����ʼ���ʵ���AΪ0.6mol�� BΪ0.3mol,CΪ1.4mol���������У��ﵽƽ���C�����������Ϊ��������z��ֵΪ
xC(g)�ﵽƽ�� ��C���������Ϊ��������ά���������ݻ����¶Ȳ��䣬����ʼ���ʵ���AΪ0.6mol�� BΪ0.3mol,CΪ1.4mol���������У��ﵽƽ���C�����������Ϊ��������z��ֵΪ
A��ֻ��Ϊ2 B��ֻ��Ϊ3 C������Ϊ2��Ҳ����Ϊ3 D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1��500��ʱ����a mol SO2��b mol O2��3��2ͨ��̶��ݻ�Ϊ5L���ܱ������С�
�ٷ�Ӧ������10minʱ�����n(SO2)��8mol��n(SO3)��4mol����b��___________mol��
�ڷ�Ӧ������10minʱ����÷�Ӧ����392kJ���������Ȼ�ѧ����ʽ�е�
��H��____________��
��10min��ƽ������v(SO2)��____________________��
�ܷ�Ӧ�ﵽƽ����������ѹǿ�Ƿ�Ӧ��ʼѹǿ��0.715������ƽ��ʱ
c(SO3)��___________________��SO2��ת���ʦ�1(SO2)��________________��
��2������Ӧ�¶ȡ���ʼSO2��O2���ʵ������루1����ͬʱ����������ͨ��һ��ѹ��Ӧ�����У���ƽ��ʱSO2��ת����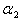 �루1����ת����
�루1����ת����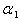 �Ĺ�ϵ��
�Ĺ�ϵ��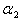 ___________
___________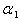 ���������)
���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�о���ѧϰС�����ⶨ������(25 �桢101 kPa)������Ħ���������ش��������⡣
��С����Ƶļ���ʵ��װ����ͼ��ʾ��

��ʵ�����Ҫ�����������£�
������100 mL 1.0 mol��L-1��������Һ��
����________(���������Ʋ�ע�����)��ȡ7.5mL 1.0 mol��L-1��������Һ������ƿ�У�
�۳�ȡa g�ѳ�ȥ��������Ĥ��þ������ϵ��ͭ˿ĩ�ˣ�ΪʹHClȫ���μӷ�Ӧ��a����ֵ����Ϊ________��
�������ƿ��װ������ˮ������ͼ���Ӻ�װ�ã����װ�õ������ԣ�
�ݷ�Ӧ���������ϵ�¶Ȼָ������£�������Ͳ��ˮ�����ΪV mL��
�뽫�������貹���������ش��������⡣
��1��������У�����100 mL 1.0 mol��L-1��������Һʱ��������Щ������ʹ����Ũ��ƫС����д��ĸ�� ��
A������Ͳ��ȡŨ����ʱ��������Ͳ�Ŀ̶�
B������ƿδ���T����������Һ
C��Ũ�������ձ���ϡ��ʱ������ʱ�����
D��������ɺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶���
E��������ƿ�ж���ʱ��������ƿ�̶���
F���ձ���������ˮ
��2������д���������еĿո����_______________�������___________
��3��ʵ�鲽�����Ӧѡ��__________(����ĸ)����Ͳ��
A��100 mL���������� B��200 mL���������� C��500 mL
��4������ʱ���ָ��������⣬��Ҫע��
��______________________________����_________________________________��
��5������ˮ����Ӱ�죬�ڸ������²������Ħ������ļ���ʽΪVm��____L/mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±����г���25�桢101kPaʱһЩ���ʵ�ȼ��������
| ���� | CH4 | C2H2 | H2 |
| ȼ���ȣ�kJ��mol��l | 890.3 | 1299.6 | 285.8 |
��֪���ܣ�C��H����413.4 kJ��mol��1��H��H����436.0 kJ��mol��1��������������ȷ����
A��C��C����Ϊ796.0 kJ��mol��1 B��C��H������С��H��H��
C��2H2(g)+O2(g)=2H2O(g) ��H=��571.6 kJ��mol��1
D��2CH4(g)=C2H2(g) +3H2(g) ��H=��376.4 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼʾ���Ӧ�������������
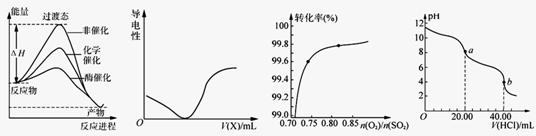
ͼ1 ͼ2 ͼ3 ͼ4
A����ͼ1��ʾ���߿�֪����ѧ����ø����Ч����
B����H2S��Һ������ʵ���У���ͼ2��ʾ���߿�ȷ��ͨ�������XΪCl2
C����������������ʱ��2SO2(g)+ O2(g) 2SO3(g)ת����ϵ��ͼ3���У��������ʾO2��ת����
2SO3(g)ת����ϵ��ͼ3���У��������ʾO2��ת����
D��ͼ4����0.l000 mol��L��1������ζ�20.00 mL 0.l000mol��L��1 Na2CO3��Һ�����ߣ���a��b�㷴Ӧ�����ӷ���ʽΪ��HCO3����H�� = CO2����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 A����ͼ��֪��A��SO2��ƽ��Ũ��Ϊ0.4 mol��L��1
A����ͼ��֪��A��SO2��ƽ��Ũ��Ϊ0.4 mol��L��1
B����ͼ��֪��B��SO2��O2��SO3��ƽ��Ũ��֮��Ϊ2��1��2
C����ƽ�����С�����ݻ�����Ӧ���ʱ仯ͼ�������ͼ�ұ�ʾ
D��ѹǿΪ0.50 MPaʱ��ͬ�¶���SO2ת�������¶ȹ�ϵ���ͼ����T2��T1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com