
【题目】某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-等,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是________________(填代号)。

(2)根据上述实验判断原溶液中肯定存在的离子是__________,肯定不存在的离子是_________。
(3)写出与②和③两个实验有关的离子方程式:
②______________________________,③_______________________________。
【答案】BD NO3-、Al3+、SO42- Fe3+、Ba2+、HCO3- 3Cu+8H++2NO3-====3Cu2++2NO↑+4H2O Al3++3NH3·H2O====Al(OH)3↓+3NH4+
【解析】
(1)用试纸检验溶液的酸碱性时,应用玻璃棒蘸取少量溶液(或用胶头滴管滴加)滴在放在玻璃片的试纸上检验;
(2)①用蓝色石蕊试纸检测该溶液,试纸显红色,说明溶液呈酸性,则一定不存在HCO3-,溶液无色,则不存在Fe3+;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色,该气体为NO,说明溶液中存在NO3-;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失,说明含有Al3+离子;
④取溶液少许,滴入氯化钡溶液产生白色沉淀,该沉淀为硫酸钡沉淀,说明含有SO42-,则一定不会含有Ba2+;
⑤取实验 ④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失,不能证明是否含有Cl-离子,因④中加入氯化钡;
根据以上分析解答。
(3)②反应为金属铜在酸性条件下与硝酸根离子发生氧化还原反应生成铜离子和一氧化氮气体,据此写出该反应的离子方程式;
③铝离子和一水合氨反应生成氢氧化铝白色沉淀和铵根离子,据此写出该反应的离子方程式。
(1)用试纸检验溶液的酸碱性时,应用玻璃棒蘸取少量溶液(或用胶头滴管滴加)滴在放在玻璃片的试纸上检验;故答案为:BD;
(2)①用蓝色石蕊试纸检测该溶液,试纸显红色,说明溶液呈酸性,则一定不存在HCO3-,溶液无色,则不存在Fe3+;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色,该气体为NO,说明溶液中存在NO3-;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失,说明含有Al3+离子;
④取溶液少许,滴入氯化钡溶液产生白色沉淀,该沉淀为硫酸钡沉淀,说明含有SO42-,则一定不会含有Ba2+;
⑤取实验 ④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失,不能证明是否含有Cl-离子,因④中加入氯化钡,
结合以上分析可知,原溶液中肯定存在的离子是NO3-、Al3+、SO42-;肯定不存在的离子是Fe3+、Ba2+、HCO3-;
综上所述,本题答案是:NO3-、Al3+、SO42-;Fe3+、Ba2+、HCO3-。
(3)②反应为金属铜在酸性条件下与硝酸根离子发生氧化还原反应生成铜离子和一氧化氮气体,反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
综上所述,本题答案是: 3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
③Al(OH)3不溶于弱碱,则在含Al3+溶液中加入足量的氨水只生成Al(OH)3,反应的离子方程式为Al3++3NH3H2O═Al(OH)3↓+3NH4+;
综上所述,本题答案是: Al3++3NH3H2O═Al(OH)3↓+3NH4+。


科目:高中化学 来源: 题型:
【题目】物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A为气体化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。若甲为淡黄色固体,D和A的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。

则(1)A的分子式是______________,甲的电子式是______________。
(2)D的溶液与乙反应的离子方程式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的正确组合是
物质分类 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | Na2SO3 | H2SO4 | NaHCO3 | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | KOH | HNO3 | CaCO3 | CaO | SO3 |
D | NaOH | CH3COOH | CaF2 | CO2 | SO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程,观察不到颜色变化的是( )
A.NO气体暴露在空气中
B.往FeCl3溶液中滴入KSCN溶液
C.Cl2通过湿润的有色布条
D.往NaOH溶液中通入CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应N2+3H2![]() 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
A. 3v正(N2)=v正(H2)B. 2v正(N2)=v逆(NH3)
C. v正(N2)=3v逆(H2)D. 2v正(H2)=3v逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.只含有一种元素的物质一定是纯净物
B.石墨在一定条件下转变为金刚石是化学变化
C.有单质参加的反应一定是氧化还原反应
D.碳元素只能形成金刚石和石墨两种同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193K,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是
A. S2Cl2的电子式为![]()
B. 固态时S2Cl2属于原子晶体
C. S2Cl2与NaOH的化学方程式可能为:S2Cl2+6NaOH=2NaCl+Na2SO3+Na2S+3H2O
D. S2Cl2是含有极性键和非极性键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液,相应的实验过程可用下图表示。请回答:
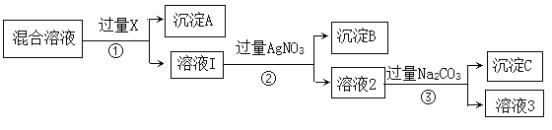
(1)沉淀A是__________(填化学式)。
(2)步骤③中加入过量Na2CO3的作用为________________________。
(3)若要获得纯净的NaNO3固体,需要向溶液3中加入过量的___________。反应的离子方程式为_______________________,反应后还需进行的实验操作为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com