
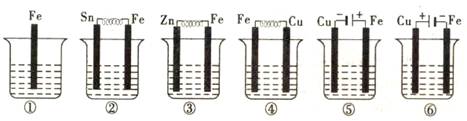


科目:高中化学 来源:不详 题型:单选题
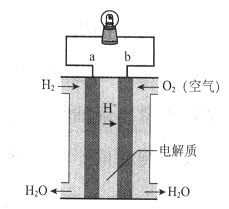
| A.a极是负极 |
| B.电子由b通过灯泡流向a |
| C.该电池总反应是2H2+ O2= 2H2O |
| D.该装置可将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镍镉电池、锂离子电池和碱性锌锰干电池都是二次电池 |
| B.燃料电池是一种高效但是会污染环境的新型电池 |
| C.化学电池的反应本质是氧化还原反应 |
| D.铅蓄电池放电的时候正极是Pb,负极是PbO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
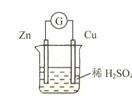
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池是一种直接把化学能转化为电能的装置,在此转化过程中无能量损耗 |
| B.在Zn-Cu-H2SO4构成的原电池中,H+不断移向负极 |
| C.钢铁在潮湿的环境中易被腐蚀与原电池有关 |
| D.纯铁比生铁(含有少量杂质)与稀HCl反应快 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | A | B | C | D |
| 正极 | Cu | Fe | Cu | C |
| 负极 | Fe | Cu | C | Cu |
| 电解质溶液 | CuSO4 | CuSO4 | FeCl3 | FeCl3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
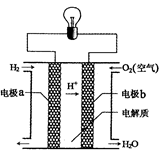
| A.该电池的总反应:2H2+O2=2H2O |
| B.该电池中电极b是负极 |
| C.外电路中电子由电极b通过导线流向电极a |
| D.该电池工作时电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池的电极只能由两种不同的金属构成 |
| B.锌锰干电池中,锌电极是正极 |
| C.手机上用的锂电池属于二次电池 |
| D.在燃料电池的正极上发生反应的常是可燃性气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com