
【题目】下列装置能达到实验目的的是( )
A.制备乙烯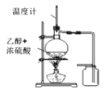
B.除去甲烷中少量的乙烯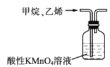
C.从碘的苯溶液中分离碘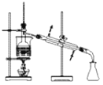
D.验证乙炔的还原性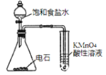
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.碳酸钡溶于盐酸溶液中:BaCO3+2H+===Ba2++H2O+CO2↑
B.小苏打溶液与氢氧化钠溶液混合:![]() +OH-===CO2↑+H2O
+OH-===CO2↑+H2O
C.氯化钙溶液与碳酸氢钾溶液混合:Ca2++![]() ===CaCO3↓
===CaCO3↓
D.硫酸铜溶液与氢氧化钡溶液混合:![]() + Ba2+===BaSO4↓
+ Ba2+===BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乳酸薄荷醇酯![]() 仅能发生水解、氧化、消去反应
仅能发生水解、氧化、消去反应
B.乙醛和丙烯醛![]() 不是同系物,但它们与氢气充分反应后的产物是同系物
不是同系物,但它们与氢气充分反应后的产物是同系物
C.蔗糖和麦芽糖在酸催化下完全水解后的产物都是葡萄糖
D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.同温同压下,1 mol N2与1 mol CO可能具有不同的体积
B.同温同压下,二氧化碳与笑气(化学式为N2O)的密度相同
C.质量相同的O2与O3,一定具有相同的原子数
D.28 g CO与1 mol CO一定具有相同的碳原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质![]() 括号内为杂质
括号内为杂质![]() ,所用的除杂试剂和分离方法都正确的是( )
,所用的除杂试剂和分离方法都正确的是( )
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
B | 溴乙烷(Br2) | NaOH溶液 | 蒸馏 |
C | 溴苯(液溴) | 乙醇 | 分液 |
D | 乙醇(水) | 新制生石灰 | 蒸馏 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H是一种广谱高效食品防腐剂,如图所示是H分子的球棍模型,下列有关说法正确的是
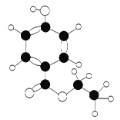
A. 有机物H的分子式为C9H11O3
B. 有机物H的官能团有羟基、羰基和醚键
C. 有机物H能发生加成反应、取代反应和氧化反应
D. 1mol有机物H最多可与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,下列四种气体的关系中,从大到小的是
①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3
A. 体积:④>①>②>③
B. 密度:②>③>④>①
C. 质量:②>①>③>④
D. 氢原子数:①>②>③>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为_______,其沸点比NH3的_______(填“高”或“低”),其判断理由是_________________________。
(2)Fe成为阳离子时首先失去______轨道电子,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为______________________。
(3)比较离子半径:F__________O2(填“大于”等于”或“小于”)。
(4)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。

图中F和O2共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为____________,通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=________g·cm3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ),则原子2和3的坐标分别为__________、__________。
),则原子2和3的坐标分别为__________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题:
(1)用分析天平准确称取该样品5.0g,全部溶于水配制成1000.0mL的溶液。用____(填一仪器名称)量取其中20.00mL放在锥形瓶中,滴加几滴指示剂,待测。该中和滴定中可选用的指示剂是__________________________,(如有几种,可任填一种)滴定终点的现象是___________________________________________________________。
(2)用0.10mol/L的盐酸溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 20.00 | 24.01 |
2 | 20.00 | 23.99 |
3 | 20.00 | 22.10 |
计算样品中,NaOH的质量百分含量为__________________。
(3)若滴定前,滴定管尖端有气泡,滴定终了气泡消失,将使所测结果______(填“偏高”、“偏低”或“不变”,下同),若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果_______;
(4)下图为0.10mol/L 25 mL NaOH溶液中逐滴滴加0.10mol/L CH3COOH溶液过程中溶液pH的变化曲线,请回答:
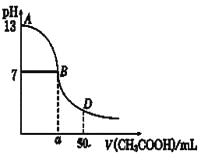
①B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?________区间。(若正确,此问不答)。
②在D点时,溶液中c(CH3COO-)+c(CH3COOH)______2c(Na+)。(填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com