
【题目】地下水受到硝酸盐污染已成为世界范围内一个相当普遍的环境问题。用零价铁去除水体中的硝酸盐(NO3-)是地下水修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。

作负极的物质是___________;正极的电极反应式是_____________。
(2)将足量铁粉投入水体中,测定NO3-去除率和pH,结果如下:

在pH =4.5的水体中,NO3-的去除率低的原因是_____________。
(3)为提高pH =4.5的水体中NO3-的去除率,某课题组在初始pH =4.5的水体中分别投入①Fe2+、②Fe、③Fe和Fe2+做对比实验结果如图:

此实验可得出的结论是____,Fe2+的作用可能是_________。(2)中NO3-去除率和铁的最终物质形态不同的原因______________。
(4)地下水呈中性,在此条件下,要提高NO3-的去除速率,可采取的措施有_______。(写出一条)
【答案】 Fe NO3-+8e-+10H+=NH4++3H2O FeO(OH)不导电,阻碍电子转移 本实验条件下,Fe2+不能直接还原NO3-,在Fe和Fe2+共同作用下能提高NO3-的去除率 Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4
初始pH低时,产生的Fe2+充足 初始pH高时,产生的Fe2+不足 减小铁粉的颗粒大小,增大反应接触面积或加入活性炭,形成微电池
【解析】(1)本题原电池中正负极的判断,活泼金属作负极,铁是活泼金属,因此负极物质为Fe,原电池中正极上发生还原反应,得到电子,根据原理,因此NO3-在正极上得到电子,转变成NH4+,因此正极电极反应式为NO3-+10e-+10H+=NH4++3H2O;(2)根据表格中铁最终物质形态,pH=4.5时FeO(OH)2全部覆盖住铁,且FeO(OH)不导电,阻碍电子转移;(3)主要原因是Fe2+水解成FeO(OH),生成Fe3O4产率降低,FeO(OH)不导电,因此NO3-的去除率低;从图中只加入铁粉和只加入Fe2+,NO3-的去除率都不如同时加入Fe2+和铁粉的高,结论是:本实验条件下,Fe2+不能直接还原NO3-,在Fe和Fe2+共同作用下能提高NO3-的去除率 ;Fe2+的作用是将不导电FeO(OH)转化成导电的Fe3O4;初始pH低时,产生的Fe2+充足,初始pH高时,产生的Fe2+不足;(4)从提高化学反应速率的因素考虑,减小铁粉的颗粒大小,增大反应接触面积或加入活性炭,形成微电池等。


科目:高中化学 来源: 题型:
【题目】将乙醇滴入热的浓硫酸中,发生反应:C2H5OH+6H2SO4=6SO2↑+2CO2↑+9H2O,浓硫酸没有体现的性质是( )
A.氧化性
B.脱水性
C.酸性
D.吸水性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既不能与氢气发生加成反应又不能使酸性高锰酸钾褪色的是:
①甲苯 ②苯酚 ③聚丙烯 ④聚乙炔 ⑤天然橡胶 ⑥苯甲醛 ⑦油脂 ⑧ 直馏汽油 ⑨葡萄糖 ⑩脲醛树脂
A. ③⑧ B. ①⑧⑩ C. ④⑤⑦⑨ D. ①②③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有CuO、Fe、H2、Ba(OH)2溶液、K2CO3溶液、NaOH溶液、稀硫酸七种物质,在常温下两种物质两两间能发生反应最多有
A.4个 B.5个 C.6个 D.7个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,CH3COOH:K=1.75×10-5,H2S:K1=1.3×10-7、K2=7.1×10-15。物质的量浓度均为0.1 mol/L的①CH3COONa溶液 ②Na2S溶液 ③NaHS溶液,三种溶液的pH由小到大的顺序是
A. ①③② B. ③①②
C. ③②① D. ②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120℃时1体积某气态烃和4体积O2混合,完全燃烧后恢复到原来的温度和压强时,体积不变,该分子式中所含的碳原子数不可能是
A. 1 B. 2 C. 3 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组欲制备漂白剂亚氯酸钠(NaClO2)。甲同学通过查阅文献发现:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体的是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
实验I 乙同学利用下图所示装置制取NaClO2晶体
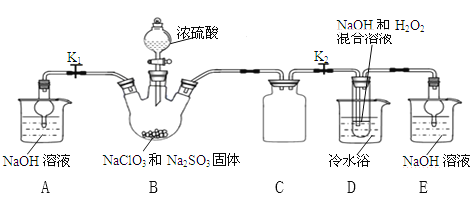
(l)装置B中使浓硫酸顺利滴下的操作是______,该装置中生成了ClO2,反应的化学方程式为_____________。
(2)装置A和E的作用是__________。
(3)装置D中发生反应的化学方程式为____________。
(4)反应结束后,先将装置D反应后的溶液在55℃条件下减压蒸发结晶,然后进行的操作是_______,再用38℃~60℃的温水洗涤,最后在低于60℃条件下干燥,得到NaClO2晶体。
实验Ⅱ 丙同学设计实验测定制得NaClO2样品的纯度
其实验步骤如下:
① 称取所得亚氯酸钠样品ag于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应后,配成100mL混合液。
② 取25.00 mL待测液于锥形瓶中,用bmol/LNa2S2O3标准液滴定,消耗标准液体积的平均值为VmL(已知:I2+2S2O32-=2I-+S4O62-)。
(5)步骤① 反应的离子方程式为______________。
(6)步骤② 滴定中使用的指示剂是_________。
(7)样品中NaClO2的质最分数为_______(用含a、b、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有两瓶失去标签的溶液,其中一瓶是Na2CO3溶液,另一瓶是NaOH溶液,浓度均未知.鉴别时,下列选用的试纸或试剂不正确的是( )
A.酚酞溶液
B.HCl溶液
C.BaCl2溶液
D.Ba(OH)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com