
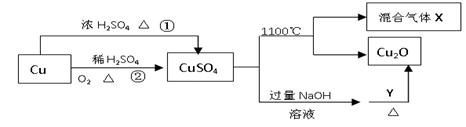
| A.相对于途径①,途径②更好地体现了绿色化学思想 |
| B.Y可以是葡萄糖溶液 |
| C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D.将CuSO4溶液蒸发浓缩,冷却结晶可制得胆矾晶体 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硫和氯水均具有漂白性,混合使用效果更好 |
| B.对滴有酚酞试液的CH3COONa溶液加热,溶液的颜色将变浅 |
| C.新能源汽车的推广与使用有助于减少光化学烟雾的产生 |
| D.用脱硫处理的煤代替原煤做燃料可以有效减少空气中CO2气体的含量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 操作和现象 | 结论 |
| A | 向NaCl溶液中先滴加少量AgNO3溶液,后滴加少量NaI溶液,先有白色沉淀,后变成黄色沉淀 | 说明Ksp(AgI)<Ksp (AgCl) |
| B | 将SO2通入酸性KMnO4溶液中,紫色褪去 | 说明SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 说明氧化性:Cu2+>Fe3+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 事实 | 解释或结论 |
| A | 常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,产生气泡 | 常温下: Ksp(BaCO3)>Ksp(BaSO4) |
| B | 盐酸与亚硫酸钠反应,生成使品红试液褪色的气体 | 非金属性:Cl> S |
| C | 滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深 | NaHCO3分解生成了Na2CO3,碱性增强 |
| D | 光束通过Al(OH)3胶体时会发生丁达尔效应 | 胶体粒子的直径为1nm~100 nm |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
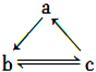
| | a | b | c |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | S | SO3 | H2SO4 |
| D | Si | SiO2 | H2SiO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com