


 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
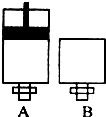 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.查看答案和解析>>
科目:高中化学 来源:2011-2012学年黑龙江庆安县第三中学高三上学期第一次月考化学试卷 题型:填空题
(20分)已知X、Y、Z、W是短周期常见非金属元素,它们的原子序数依次增大,X元素原子形成的离子就是一个质子,Z、W在周期表中处于相邻位置,它们的单质在常温下都是气体,Y原子的最外层电子数是内层电子数的2倍。
(1)写出元素符号:X____、Y____、Z____、W____。
(2)、按X、Y、Z、W的顺序,这四种元素可组成原子个数比为5:1:1:3的化合物,该化合物与足量的氢氧化钠溶液反应的离子方程式为________。
(3)、将9gY单质在足量W单质中燃烧,所得气体通入1L1mol/LNaOH溶液中,充分反应后溶液中含的溶质有(填化学式)________,其物质的量分别是________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省温州市十校联考高二(下)期中化学试卷(解析版) 题型:选择题
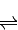 H++CH3COO-,下列叙述不正确的( )
H++CH3COO-,下列叙述不正确的( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com