
【题目】I.实验室制备、收集干燥的 SO2,所需仪器如下图。
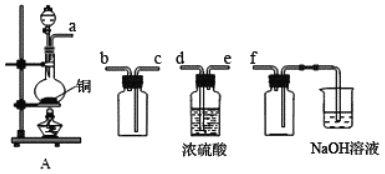
(1)装置A产生SO2,按气流方向连接各仪器接口,顺序为 a→___→___→___→___→f。
(2)验证产生的气体是 SO2的方法及实验现象是_________________________________。
(3)若在1 L 0.3 mol/L的 NaOH溶液中,通入4.48 L SO2(标况),反应后所得溶液中微粒的浓度之间有一些等量关系,例如:c(Na+)+ c(H+)= c(HSO3-)+2 c(SO32-)+ c(OH-),请再写出两个等量关系: ________________。
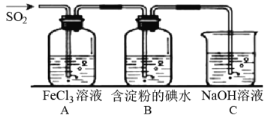
II.SO2 气体为无色气体,有强烈刺激性气味,大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如下图所示:
(4)若要从FeCl3溶液中提取晶体,必须进行的实验操作步骤中没有用到的玻璃仪器有_________。
a.酒精灯 b.烧瓶 c.漏斗 d.烧杯 e.玻璃棒
(5)装置 A 中的现象是_________________,写出 B 中发生反应的离子方程式:___________________。
(6)在上述装置中通入过量的 SO2,为了验证A中SO2与 Fe3+发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入 KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案中不合理的是________。
【答案】
(1)d→e→c→b;
(2)将气体通入品红溶液,溶液褪色,加热恢复原色;
(3)2c(Na+) =3[c(SO32-)+ c(HSO3-)+ c(H2SO3)]
c(SO32-)+ c(HSO3-)+ c(H2SO3)=0.2mol/L
c(HSO3-)+3 c(H2SO3)+2 c(H+)= c(SO32-)+2 c(OH-)
(4)b
(5)溶液颜色由黄色逐渐变为浅绿色;I2+SO2+2H2O = 2I-+SO42-+4H+
(6)①
【解析】
试题分析:(1)收集二氧化硫应先干燥再收集,故先通过d、e,二氧化硫的密度比空气大,要从c口进气,b口出来进行尾气处理.因为二氧化硫易于氢氧化钠反应,故f的作用是安全瓶,防止倒吸;盛放NaOH溶液的烧杯为尾气处理装置要放置在最后;故答案为:d;e;c;b;
(2)检验二氧化硫的一般方法是将气体通入品红溶液中,如果品红褪色,加热后又恢复红色,证明有二氧化硫,故答案为:将气体通入品红溶液中,如果品红褪色,加热后又恢复红色;
(3)n(NaOH)=0.3mol/L×1L=0.3mol,n(SO2)=![]() =0.2mol,设生成Na2SO3、NaHSO3的物质的量分别是xmol、ymol,根据Na、S原子守恒得x+y=0.22x+y=0.3解得,x=0.1mol,y=0.1mol,所以溶液中的溶质是等物质的量的Na2SO3、NaHSO3,溶液中存在电荷守恒、物料守恒和质子守恒,根据电荷守恒得c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-),根据物料守恒得2c(Na+)=3c(HSO3-)+3c(SO32-)+3c(H2SO3),]),[SO32-]+[HSO3-]+[H2SO3]=0.2mol/L,根据质子守恒得c(HSO3-)+3c(H2SO3)+2c(H+)=c(SO32-)+2c(OH-),故答案为:2c(Na+)=3c(HSO3-)+3c(SO32-)+3c(H2SO3),[SO32-]+[HSO3-]+[H2SO3]=0.2mol/L或c(HSO3-)+3c(H2SO3)+2c(H+)=c(SO32-)+2c(OH-);
=0.2mol,设生成Na2SO3、NaHSO3的物质的量分别是xmol、ymol,根据Na、S原子守恒得x+y=0.22x+y=0.3解得,x=0.1mol,y=0.1mol,所以溶液中的溶质是等物质的量的Na2SO3、NaHSO3,溶液中存在电荷守恒、物料守恒和质子守恒,根据电荷守恒得c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-),根据物料守恒得2c(Na+)=3c(HSO3-)+3c(SO32-)+3c(H2SO3),]),[SO32-]+[HSO3-]+[H2SO3]=0.2mol/L,根据质子守恒得c(HSO3-)+3c(H2SO3)+2c(H+)=c(SO32-)+2c(OH-),故答案为:2c(Na+)=3c(HSO3-)+3c(SO32-)+3c(H2SO3),[SO32-]+[HSO3-]+[H2SO3]=0.2mol/L或c(HSO3-)+3c(H2SO3)+2c(H+)=c(SO32-)+2c(OH-);
(4)操作步骤:蒸发需用到酒精灯、蒸发皿、玻璃棒,冷却结晶需用到烧杯,过滤需用到漏斗、烧杯、玻璃棒,故不需要B.烧瓶,故答案为:B;
(5)装置 A 中反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,溶液颜色由黄色逐渐变为浅绿色;B 中二氧化硫与碘水反应生成氢碘酸和硫酸,发生反应的离子方程式为I2+SO2+2H2O = 2I-+SO42-+4H+,故答案为:溶液颜色由黄色逐渐变为浅绿色;I2+SO2+2H2O = 2I-+SO42-+4H+;
(6)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,所以不合理的是方案①,因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色,故答案为:①;


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
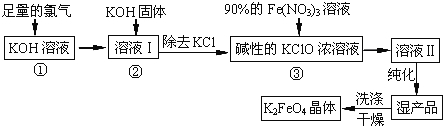
(1)反应①应在温度较低的情况下进行.因在温度较高时KOH 与Cl2 反应生成的是KClO3.写出在温度较高时KOH 与Cl2反应的化学方程式 ;
(2)在反应液I中加入KOH固体的目的是 (填编号);
A.与反应液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为 。
(4)如何判断K2FeO4晶体已经洗涤干净 。
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,其离子反应是: FeO42﹣+ H2O= Fe(OH)3(胶体)+ O2↑+
完成并配平上述反应的离子方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某人设计淀粉利用方案如图所示。其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:
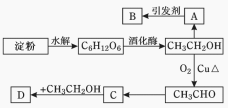
(1)C6H12O6的名称是________,A的电子式为_________,C中含有官能团名称 ;
(2)A→B反应类型____________;C→D反应类型____________。
(3)写出下列转化的化学方程式:
① A→B:______________________________________________________;
② A→CH3CH2OH:______________________________________;
③ C→D:_____________________________________________________;
④ CH3CH2OH→CH3CHO:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)已知反应CO(g)+2H2(g)![]() CH3OH(g) ΔH=-99kJ·mol-1中的相关化学键能如下:
CH3OH(g) ΔH=-99kJ·mol-1中的相关化学键能如下:
![]()
则x= 。
(2)甲醇作为一种重要的化工原料,既可以作为燃料,还可用于合成其它化工原料。在一定条件下可利用甲醇羰基化法制取甲酸甲酯,其反应原理可表示为:CH3OH(g) +CO(g) ![]() HCOOCH3(g) ΔH=-29.1kJ·mol-1。向体积为2L的密闭容器中充入2mol CH3OH(g) 和2mol CO,测得容器内的压强(p:kPa)随时间(min)的变化关系如下图中Ⅰ、Ⅱ、Ⅲ曲线所示:
HCOOCH3(g) ΔH=-29.1kJ·mol-1。向体积为2L的密闭容器中充入2mol CH3OH(g) 和2mol CO,测得容器内的压强(p:kPa)随时间(min)的变化关系如下图中Ⅰ、Ⅱ、Ⅲ曲线所示:

①Ⅱ和Ⅰ相比,改变的反应条件是 。
②反应Ⅰ在5min时达到平衡,在此条件下从反应开始到达到平衡时v(HCOOCH3)= 。
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ) = 。在体积和温度不变的条件下,在上述反应达到平衡Ⅱ时,再往容器中加入1mol CO和2mol HCOOCH3后v(正) v(逆)(填“﹥”“﹤”“﹦”),原因是 。
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1 T3(填“﹥”“﹤”“﹦”),判断的理由是 。
(3)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2。某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如下图所示,利用以下反应填空:
NO+CO![]() N2+ CO2(有CO) 2NO
N2+ CO2(有CO) 2NO![]() N2+ O2(无CO)
N2+ O2(无CO)
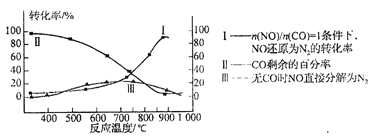
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为 。
②在n(NO)/ n(CO)=1的条件下,应控制最佳温度在 左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝硅合金材料性能优良。铝土矿(含 30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该合金的工艺如下:
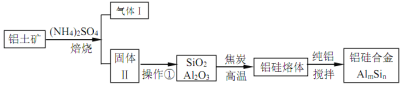
(1)铝硅合金材料中若含铁,会影响其抗腐蚀性。原因是______________。
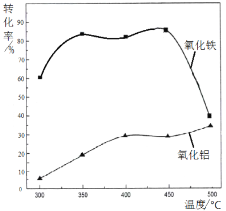
(2)焙烧除铁反应时 Fe2O3 转化为NH4Fe(SO4)2,Al2O3少部分发生类似反应。写出 Fe2O3发生反应的方程式:______________。 氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为______________。
(3)若操作①中所得溶液中加入过量NaOH 溶液,含铝微粒发生反应的离子方程式为:______________。
(4)用焦炭还原SiO2、Al2O3会产生SiC等中间体。写出中间体 SiC 再与Al2O3反应生成铝、硅单质的化学方程式并表出电子转移的方向和数目:______________ 。
(5)已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38。向 FeCl3和 AlCl3的混合溶液中逐滴加入NaOH 溶液,生成 Al(OH)3和Fe(OH)3沉淀,当两种沉淀共存时,上层溶液中 c(Al3+):c(Fe3+)=__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH) 2CO3等杂质]为原料制取二氧化锰,其流程示意图如下:
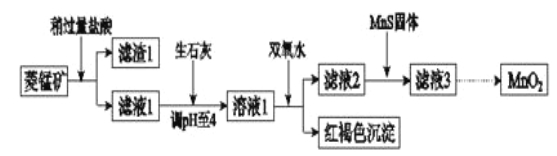
已知:生成氢氧化物沉淀的pH
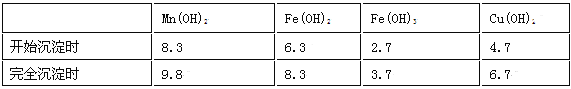
注:金属离子的起始浓度为0.1 mol/L,回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是 _______ ___________ 。盐酸溶解MnCO3的化学方程式是_______ ______________ ___ _____。
(2)向溶液1中加入双氧水时,反应的离子方程式是 _______ ___________ 。
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是 ________ 。
(4)将MnCl2转化为MnO2的一种方法是氧化法。其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:□Mn2++□ClO3-+□________=□________+□________+□________。
(5)将MnCl2转化为MnO2的另一种方法是电解法。
① 阳极生成MnO2的电极反应式是 ____ ___ ____________ _______ 。
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2。检验Cl2的操作是 _____ 。
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生。其原因是 ___ __ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物
(1)工业上尿素由CO2和NH3合成,写出其方程式 ___________________________.
(2)当氨碳比![]() 时,CO2的转化率随时间的变化关系如图所示。
时,CO2的转化率随时间的变化关系如图所示。

①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”)。
②NH3的平衡转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
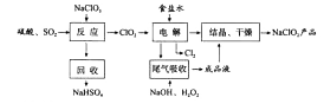
回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式_______。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
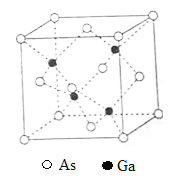
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com