
| A. | 聚乙烯塑料制品可用于食品的包装 | |
| B. | 石油催化裂化的主要目的是提高汽油等轻质油的产量与质量 | |
| C. | 原电池放电发生化学变化,同时能量发生转化 | |
| D. | 开发太阳能,推广使用甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 |
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:填空题
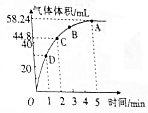 取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)
取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略) | 序号 | 条件 | 现象和结论 | |
| 温度/℃ | 催化剂 | ||
| 1 | 40 | FeCl3溶液 | |
| 2 | 20 | FeCl3溶液 | |
| 3 | 20 | MnO2 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
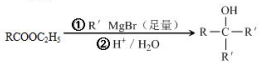
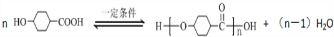 .
. .
.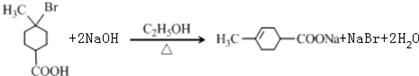 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
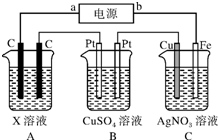 如图所示,电解一段时间后,测得C中Ag+减少了0.1mol,Fe电极被溶解.试回答:
如图所示,电解一段时间后,测得C中Ag+减少了0.1mol,Fe电极被溶解.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFeBr2与1molCl2反应时转移的电子数为1NA | |
| B. | 10g H218O与D216O的混合物中所含中子、电子数目均为5NA | |
| C. | 标况下,22.4L甲烷中含有C-H键数为1NA | |
| D. | pH=2的H2SO4溶液1L,含H+的数目为0.02NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 火力发电中,燃烧是使化学能转换为电能的关键 | |
| C. | 塑胶跑道的主要成分聚氨酯属于有机高分子化合物 | |
| D. | 原子经济性反应是绿色化学的重要内容 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
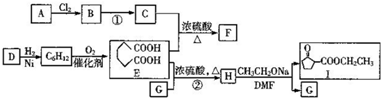
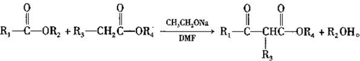
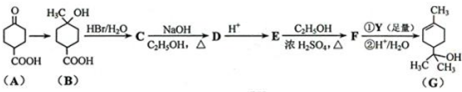
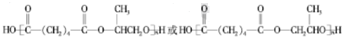 ,1中官能团的名称酯基和羰基.
,1中官能团的名称酯基和羰基.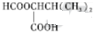 .
.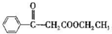 写出合成路线图.
写出合成路线图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:C>A | |
| B. | 离子半径:D3+>B2- | |
| C. | 非金属性:A>B | |
| D. | 最高价氧化物对应水化物的碱性:C<D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com