
下列图示与对应的叙述相符的是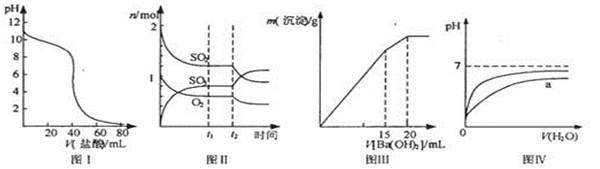
| A.图I表示盐酸滴加到0.1mol/L某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
B.图II表示一定条件下进行的反应2SO2 +O2 2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 |
| C.图III表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| D.图IV表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应 的是盐酸 |
B
解析试题分析:A、图Ⅰ表示的碱溶液pH<13,说明是弱碱溶液;反应后是强酸弱碱溶液,宜选择酸性变色突变的甲基橙,而不是碱性变色突变的酚酞作指示剂,错误; B、图Ⅱ表示的各自量不变,平衡正向移动,可能是加压过程,正确;C.明矾溶液中加入Ba(OH)2溶液的拐点方程式是2KAl(SO4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4、KAl(SO4)2+2Ba(OH)2═KAlO2+2BaSO4↓+2H2O,同样2mol KAl(SO4)2,按前者反应产生的沉淀质量是(2×78+3×233)g=855g,按后者反应产生的沉淀质量是4×233g=932g,图象形态正确,20mL Ba(OH)2溶液时,铝离子恰好变成AlO2-,错误;D.盐酸与醋酸的稀释,pH变化大的是盐酸,错误.
考点:本题考查了中和滴定、离子方程式的有关计算、物质的量或浓度随时间的变化曲线、弱电解质在水溶液中的电离平衡等知识,要求学生能正确识别图像。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
实验室需配制一种仅含五种离子(忽略水电离出的离子)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为5 mol/L,下面四个选项中能达到此目的的是( )
| A.Na+、K+、SO42?、NO3?、Cl? |
| B.Fe2+、H+、Br?、NO3?、Cl? |
| C.Ca2+、K+、OH?、Cl?、NO3? |
| D.Al3+、Na+、Cl?、SO42?、NO3? |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向10mL 0.1mol·L-1 (NH4)Al(SO4)2溶液中滴加等浓度Ba(OH)2溶液x mL。下列表述正确的是
| A.x=10时,溶液中有NH4+、Al3+、SO42-,且c(SO42-)>c(NH4+)>c(Al3+) |
| B.x=20时溶液导电能力比x=15时溶液导电能力强 |
| C.x=25时,溶液中主要有Ba2+、AlO2-,c(Ba2+)>c(AlO2-) |
| D.x=30时的离子方程式:NH4++Al3++2SO42-+2Ba2++5OH-→AlO2-+2BaSO4↓+NH3?H2O+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验过程中反应的离子方程式的书写正确的是
| A.水壶中水垢用食醋除去:2H++ CaCO3= Ca2++CO2↑+H2O 2H++Mg(OH)2= Mg2++2H2O |
| B.“84消毒液”(有效成分HClO)和 “洁厕灵”(主要成分盐酸)混用会导致氯气中毒Cl–+ClO–+2H+= Cl2↑+H2O |
| C.SO2通入滴加酚酞的NaOH溶液中,红色变浅:SO2+2NaOH=Na2SO4+ H2O |
| D.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+Fe2++14H+=2Cr3++ Fe3++7 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组离子在溶液中能够大童共存,当溶液中的pH=1时,有气体产生;而当溶液中的pH=13时,又能生成沉淀。则该组离子可能是:
| A.Na+、K+、AlO2-、CO32- | B.Fe2+、Na+、SO42-、NO3- |
| C.Mg2+、NH4+、CO32-、Cl- | D.Ba2+、K+、Cl-、MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.能使甲基橙试液显红色的溶液:Na+、NH4+、Fe3+、NO3— |
| B.能使苯酚变紫色的溶液:K+、Mg2+、I-、SO42- |
| C.含Al3+的溶液:NH4+、K+、HCO3-、Cl- |
| D.水电离产生的c(OH-)=1×10-11mol/L的溶液:Cu 2+、SO42-、NO3-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com