
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如表所示。下列说法中,正确的是( )
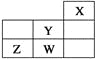
A. W的最高价氧化物对应的水化物是强酸
B. Y的原子半径在同周期主族元素中最大
C. 还原性:W->Z2-
D. Z的气态氢化物的稳定性在同主族元素中最强
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】氨对人类的生产生活具有重要影响。
(1)氨的制备与利用。
① 工业合成氨的化学方程式是 。
② 氨催化氧化生成一氧化氮反应的化学方程式是 。
(2)氨的定量检测。
水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:
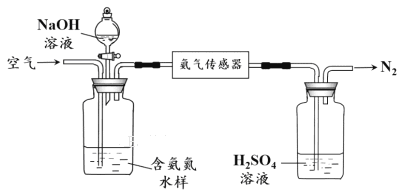
① 利用平衡原理分析含氨氮水样中加入NaOH溶液的作用: 。
② 若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol ,则水样中氨氮(以氨气计)含量为 mg·L-1。
(3)氨的转化与去除。
微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的氮转化系统原理示意图。
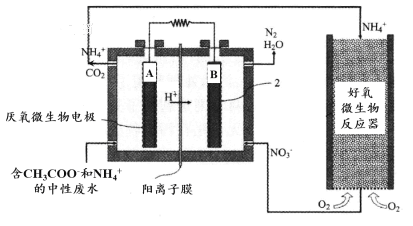
① 已知A、B两极生成CO2和N2,写出A极的电极反应式: 。
② 用化学用语简述NH4+去除的原理: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势,如图所示:
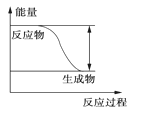
(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是_____(填字母)。
A.改铁片为铁粉 B.增大压强
C.升高温度 D.改稀硫酸为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______极(填“正”或“负”)。铜片上产生的现象为________________;该极上发生的电极反应为______________;外电路中电子由 _______极向_______极移动。(填“正”或“负”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是中学化学常用的试剂。工业上用软锰矿制备高锰酸钾流程如下:
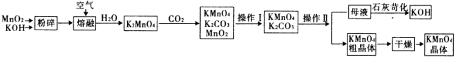
(1)铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋的还原产物为Bi3+),Mn2+的氧化产物为MnO4-,写出反应的离子方程式_________________________________________。
(2)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是_____(填代号)。
a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
(3)上述流程中可以循环使用的物质有氢氧化钾和_______(写化学式)。
(4)理论上(若不考虑物质循环与制备过程中的损失)1 mol MnO2可制得_____mol KMnO4。
(5)该生产中需要纯净的CO2气体。写出实验室制取CO2的化学方程式___________________,所需气体发生装置可以是______(选填代号)。
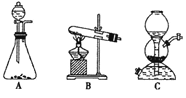
(6)操作Ⅰ的名称是________;操作Ⅱ根据 KMnO4和K2CO3两物质在______(填性质)上的差异,
采用__________(填操作步骤)、趁热过滤得到 KMnO4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫-氨热化学循环制氢示意图如下:
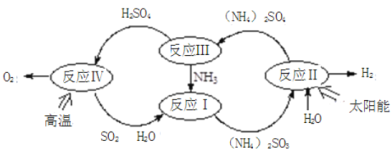
(1)反应Ⅱ是将太阳能转化为电能,再转化为化学能,电解池阳极的电极反应式 _______________;
(2)反应Ⅲ中控制反应条件很重要,不同条件下硫酸铵分解产物不同。连接装置A-B-C,检查气密性,按图示重新加入试剂。通入N2排尽空气后,于400℃加热装置A 至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2。观察到装置A、B之间的导气管内有少量白色固体。经检验,该白色固体和装置B内溶液中有SO32-,无SO42-。进一步研究发现,气体产物中无氮氧化物。
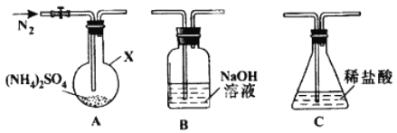
(NH4)2 SO4在400℃分解的化学方程式是:________________________________________;
(3)反应Ⅳ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O (l) △H=+462kJ/mol
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177kJ/mol
ii.SO3(g)分解。
iii.H2O(l)=H2O(g) △H=+44kJ/mol
①L(L1、L2),X可分别代表压强或温度。下图表示 L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
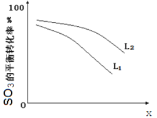
i.X代表的物理量是:________________,
ii.判断L1、L2的大小关系,并简述理由:________________________________________;
②反SO3分解的热化学方程式为:__________________________________________________;
(4)恒温密闭容器中,控制不同温度进行SO3分解实验。SO3起始浓度均为 cmol·L-1,测定SO3的转化率,结果如图,图中Ⅰ曲线为SO3的平衡转化率与温度的关系,Ⅱ曲线表示不同温度下反应经过相同反应时间且未达到化学平衡时SO3的转化率。
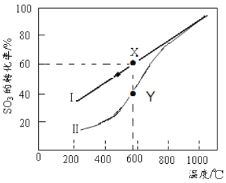
①图中点X点平衡常数:K=_____ ;
②Y点对应温度下的反应速率:v(正)______v(逆)(选填:>,<,=);随温度的升高,Ⅱ曲线逼近Ⅰ曲线的原因是:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B两种烃,已知A的分子式为C5Hm,而B的最简式为C5Hn(m、n均为正整数).请回答下列问题:
(1)下列关于烃A和烃B的说法不正确的是 (填序号).
a.烃A和烃B可能互为同系物
b.烃A和烃B可能互为同分异构体
c.当m=12时,烃A一定为烷烃
d.当n=11时,烃B可能的分子式有2种
(2)若烃A为链烃,且分子中所有碳原子一定共面,在一定条件下,1mol A最多可与1mol H2加成,则A的名称是 .
(3)若烃B为苯的同系物,取一定量的烃B完全燃烧后,生成物先通过足量的浓硫酸,浓硫酸的质量增加1.26g,再通过足量的碱石灰,碱石灰的质量增加4.4g,则烃B的分子式为 ;若其苯环上的一溴代物只有一种,则符合此条件的烃B有 种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯。回答下列问题:
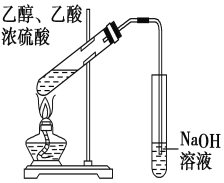
(1)写出制取乙酸乙酯的化学反应方程式 。
(2)浓硫酸的作用是: 。
(3)实验装置图有明显错误,请指出错误是 。
(4)实验中可以观察到的现象是________________________ _____________ 。
(5) 写出把制得的乙酸乙酯分离出来所需的试剂和方法 。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,
就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
②单位时间里,生成1mol乙酸乙酯,同时生成1mol水
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④混合物中各物质的浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是
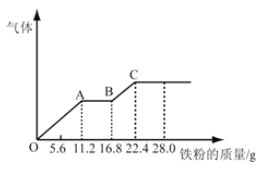
A.混合酸中NO3-物质的量为0.4mol
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.H2SO4浓度为5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 利用金属活性的不同,可以采取不同的冶炼方法冶炼金属。下列反应所描述的冶炼方法不可能实现的是( )
A.2Al2O3(熔融) ![]() 4Al+3O2↑
4Al+3O2↑
B.Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
C.Fe+CuSO4 ===FeSO4+Cu
D.2NaCl(水溶液)![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com