
【题目】将1molI2和2molH2(g)置于某2L密闭容器中,在—定温度下发生反应:I2(g)+H2(g)![]() 2HI(g) △H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线
2HI(g) △H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线

(1)达平衡时,I2(g)的物质的量浓度为 _______。H2(g)的平衡转化率为___________。
在此温度下,该反应的平衡常数K__________(保留一位小数)。
(2)若改变反应条件下,在甲条件下ω(HI)的变化如图曲线(I)所示,在乙条件下ω(HI)的变化如图曲线(III)所示。则甲条件可能是______(填入下列条件的序号。下同),乙条件可能是________。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g)、b mol H2和c mol HI(a、b、 c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的应满足的关系是_______________ (用含一个a、b、c的代数式表示)
【答案】 0.05mol/L 45% 29.5 ③⑤ ④ 2 (a+c/2)=(b+c/2) 或4a-2b+c=0
【解析】试题分析:本题考查化学平衡和化学平衡常数的计算,图像分析以及等效平衡。
(1)设起始到平衡时转化H2物质的量为x,用三段式
I2(g)+H2(g)![]() 2HI(g)
2HI(g)
n(起始)(mol) 1 2 0
n(转化)(mol) x x 2x
n(平衡)(mol) 1-x 2-x 2x
由图知平衡时ω(HI)=0.60,则![]() =0.60,解得x=0.9mol,达平衡时I2(g)的物质的量浓度为(1-0.9)mol
=0.60,解得x=0.9mol,达平衡时I2(g)的物质的量浓度为(1-0.9)mol![]() 2L=0.05mol/L。H2的平衡转化率为0.9mol
2L=0.05mol/L。H2的平衡转化率为0.9mol![]() 2mol=0.45。此温度下的平衡常数K=c2(HI)/[c(H2)·c(I2)=0.92/(0.05
2mol=0.45。此温度下的平衡常数K=c2(HI)/[c(H2)·c(I2)=0.92/(0.05![]() 0.55)=29.5。
0.55)=29.5。
(2)由图可见,曲线(I)先于曲线(III)出现拐点,甲的反应速率快,甲的条件比乙高;曲线(I)、曲线(III)平衡时ω(HI)相等,说明改变条件平衡不发生移动,该反应反应前后气体分子数相等,所以改变的条件可能是改变压强或使用催化剂;结合上述分析,甲条件可能是③恒温条件下,缩小反应容器体积和⑤恒温恒容条件下,加入适当催化剂,乙条件可能是④恒温条件下,扩大反应容器体积。
(3)达平衡时HI的体积分数仍为0.60,与原平衡时HI的体积分数相同,则两种条件下互为等效平衡;本题的特点是恒温恒容下反应前后气体分子数相等的反应,起始各物质的量一边倒转化后应成比例, ![]() =
=![]() ,即2 (a+c/2)=(b+c/2) 或4a-2b+c=0。
,即2 (a+c/2)=(b+c/2) 或4a-2b+c=0。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液,下图是医院给病人输液时使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液的标签.某学生欲在实验室中配制500mL该葡萄糖注射液. 
实验用品:葡萄糖固体、蒸馏水、烧杯、容量瓶(500mL)、药匙、胶头滴管、量筒.
(1)还缺少的仪器有 .
(2)下列对容量瓶及使用的描述中不正确的是 .
A.容量瓶上标有容积、温度和浓度
B.使用前要检查容量瓶是否漏水
C.容量瓶用蒸馏水洗净后,再用5%葡萄糖注射液洗
D.配制溶液时,把称好的葡萄糖晶体小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
(3)实验中需取用固体的质量为g,该葡萄糖注射液的物质的量浓度mol/L.
(4)配制该葡萄糖注射液,下列操作会导致所配溶液的物质的量浓度偏高的是 .
A.没有将洗涤液转移到容量瓶
B.定容时俯视刻度线
C.容量瓶洗净后未干燥
D.定容时液面超过了刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一种泉水,取0.5L这种泉水作为样品,经测定该样品中含有0.48g的Mg2+ . 那么,该泉水中Mg2+的物质的量的浓度是多少?为使该泉水样品所含的Mg2+全部沉淀,应加入1mol/L NaOH溶液的体积是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的海水综合利用的工业流程图,判断下列说法正确的是

已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A. 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B. 在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 在过程④、⑥反应中每氧化0.2 mol Br-需消耗2. 24 L Cl2
D. 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液溶质物质的量浓度为1 mol/L
C.0.5 L 2 molL﹣1的BaCl2溶液中,Ba2+和Cl﹣的总数为3×6.02×1023
D.10 g 98%的硫酸(密度为1.84 gcm﹣3)与10 mL18.4 molL﹣1的硫酸的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200mL 0.3molL﹣1的K2SO4溶液和100mL 0.2molL﹣1的Fe2(SO4)3溶液混合后,若忽略液体混合时体积的变化,则溶液中SO ![]() 的物质的量浓度为( )
的物质的量浓度为( )
A.0.3 molL﹣1
B.0.4 molL﹣1
C.0.45 molL﹣1
D.0.5 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对电解原理进行实验探究。
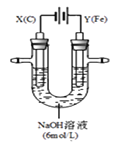
请回答:
用如图所示装置进行实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42—)在溶液中呈紫红色。
(1)电解过程中,X极区溶液的pH________(填“增大”、“减小”或“不变”);
(2)电解过程中,Y极发生的电极反应为Fe-6e—+8OH—═FeO42—+4H2O 和 4OH——4e—═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少_________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com