
A、硫离子的原子结构示意图  | ||
| B、氯离子的电子式:Cl- | ||
C、原子核内有10个中子的氧原子:
| ||
| D、二氧化硫溶于水的反应化学方程式:SO2+H2O═H2SO4 |
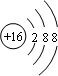 ,故A错误;
,故A错误; ,故B错误;
,故B错误;18 8 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、锌与硫酸铜溶液反应:Zn+Cu2+=Zn2++Cu |
| B、氢氧化钠溶液与盐酸反应:OH-+H+=H2O |
| C、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、氯化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
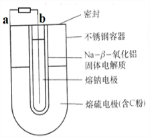
| A、a为电池的正极 |
| B、充电时b接电源的正极 |
| C、正极反应为:nS8+16ne-=8Sn2- |
| D、Na+可以穿过固体电解质和硫反应从而传递电流 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,2.24 L SO2中约含有0.1NA个分子 |
| B、常温常压下,32g氧气和32g臭氧所含氧原子总数为2NA |
| C、18g D2O所含有的电子数为10NA |
| D、5.6gFe与足量Cl2反应转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0L1.0mol/L的Na2SO4水溶液中含有的氧原子数为4NA |
| B、1molNa2O2固体中含离子总数与1molCH4中所含共价键数目相等 |
| C、1molNaClO中所有ClO-的电子总数为26NA |
| D、标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2和KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示.下列说法不正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2和KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示.下列说法不正确的是( )| A、反应I2(aq)+I-(aq)?I3-(aq)的△H<0 |
| B、状态A与状态B相比,状态A的c(I2)大 |
| C、若反应进行到状态D时,一定有V正>V逆 |
| D、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
| A、反应在前5min的平均速率为v (SO2)=0.08mol?L-1?min-1 |
| B、保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,v (正)>v (逆) |
| C、该温度,反应的平衡常数为11.25L?mol-1 |
| D、相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com