
【题目】实验室欲用氢氧化钠固体配制1.0 mol·L-1的氢氧化钠溶液240 mL。
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为__________(填序号)。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、____________________。
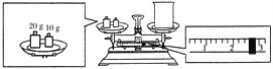
(2)某同学欲称量氢氧化钠的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如下图所示。烧杯的实际质量为__________g,要完成本实验该同学应称出____________g 氢氧化钠。
(3)使用容量瓶前必须进行的一步操作是__________。
(4)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是_________(填字母)。
A.转移溶液时不慎有少量洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
【答案】②①③⑧⑤⑥④⑦⑨ 250 mL容量瓶、胶头滴管 27.4 10.0 检查容量瓶是否漏液 BC
【解析】
(1)根据配制原理分析操作步骤和需要的仪器;
(2)根据托盘天平的原理以及m=cVM解答;
(2)使用容量瓶前必须进行的一步操作是查漏;
(4)根据c=n/V分析误差。
(1)实验室中没有240mL的容量瓶,配制时需要选用250mL的容量瓶,配制250mL1.0mol/L的NaOH溶液的步骤为:计算→称量→溶解、冷却→移液→定容→摇匀→装瓶→贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,所以正确的操作顺序为:②①③⑧⑤⑥④⑦⑨;需要的仪器除托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管之外,还缺少250mL容量瓶、胶头滴管;
(2)根据图示可知,游码的读数为2.6g,结合托盘天平的称量原理可知,图示中,砝码质量=烧杯质量+游码质量,所以烧杯质量=砝码质量-游码质量=20g+10g-2.6g=27.4g;配制250mL1.0mol/L的NaOH溶液,需要氢氧化钠的质量为:0.25L×1mol/L×40g/mol=10.0g;
(3)容量瓶有瓶塞,配制过程中需要摇匀,为了避免液体流出,配制溶液之前需要检查此容量瓶是否漏水;
(4)A、转移溶液时不慎有少量洒到容量瓶外面,导致配制的溶液中溶质的物质的量偏小,溶液浓度偏低;
B、定容时俯视刻度线,导致加入的蒸馏水体积低于容量瓶刻度线,配制的溶液体积偏小,溶液浓度偏高;
C、未冷却到室温就将溶液转移到容量瓶并定容,热的溶液体积偏大,冷却后溶液体积变小,导致配制的溶液体积偏小,溶液浓度偏高;
D、定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致配制的溶液体积偏大,溶液浓度偏低。
答案选BC。


科目:高中化学 来源: 题型:
【题目】从实验测得不同物质中氧氧之间的键长和键能的数据:
O—O键 数据 | O | O | O2 | O |
键长(10-12 m) | 149 | 128 | 121 | 112 |
键能(kJ·mol-1) | x | y | z=494 | w=628 |
其中x、y的键能数据尚未测定,但可根据规律性推导键能的大小顺序为w>z>y>x;该规律性是
A.成键的电子数越多,键能越大
B.键长越长,键能越小
C.成键所用的电子数越少,键能越大
D.成键时电子对越偏移,键能越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
①江河入海口三角洲的形成通常与胶体的性质有关
②“钡餐”中使用的硫酸钡是弱电解质
③冰和干冰既是纯净物又是化合物
④雾是气溶胶,在阳光下可观察到丁达尔现象
⑤某无色溶液中加入稀盐酸,产生的气体可使澄清石灰水变浑浊,则原溶液中一定含CO![]()
⑥可用渗析法分离Fe(OH)3胶体和KCl溶液
A. ①③④⑤ B. ①③④⑥ C. ①③④⑤⑥ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。
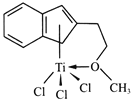
①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。
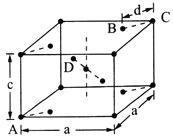
①A、B、C、D 4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用足量的一氧化碳还原4.64 g某金属氧化物,把生成的二氧化碳全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0 g,则此金属氧化物是下列中的( )
A. 氧化铜 B. 氧化铁 C. 四氧化三铁 D. 二氧化锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氧化铁样品中含有少量的硫酸亚铁。某同学要测定其中铁元素的质量分数,设计了如下实验方案。

(1)操作Ⅰ中配制溶液时,所用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管以外,还必须有__________(填仪器名称)。
(2)反应①中加入足量H2O2溶液,反应的离子方程式:_______________________________。
(3)检验沉淀中![]() 是否洗涤干净的操作是_______________________________________。
是否洗涤干净的操作是_______________________________________。
(4)将沉淀加热,冷却至室温,用天平称量坩埚与加热后固体的总质量为b1g,再次加热并冷却至室温称其质量为b2g,若b1-b2=0.3,还应进行的操作是_____________________。
(5)坩埚的质量为42.6 g,最终坩埚与加热后的固体的总质量为45.8 g,则样品中铁元素的质量分数为________________。
(6)有同学认为上述方案的实验步骤太繁琐,他认为,只要将样品溶于水充分搅拌,加热、蒸干、灼烧称量即可测得样品中铁元素的质量分数,你认为他的这个方案是否可行?__________(填“可行”或“不可行”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1mol/LNaOH溶液分别滴加到0.1mol/LHA溶液和HB溶液中,两混合溶液中离子浓度与pH的变化关系如图所示,下列说法不正确的是
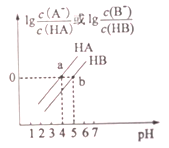
A. Ka(HB)<Ka(HA)
B. a点时,c(A-)=c(HA)>c(Na+)>c(H+)>c(OH-)
C. 常温下,0.1mol/LNaA溶液的pH大于0.1mol/LNaB溶液的pH
D. 向HB溶液中加入NaOH溶液,混合溶液中c(B-)/c(HB)=10[pH-pKa(HB)](已知:pKa=-lgKa)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修5:有机化学基础]铃兰醛具有甜润的百合香味,对皮肤的刺激性小,对碱稳定,广泛用于百合、丁香、玉兰、茶花以及素心兰、东方型香型日用香精的合成。常用作肥皂、洗涤剂的香料,还可用作花香型化妆品的香料。其合成路线如下图所示:

(1)B中官能团的名称是 ;
(2)④的反应类型是 ;
(3)写出反应②的化学方程式 ;
(4)乌洛托品的结构式如图所示,其二氯取代物有 种;

将甲醛的水溶液与氨水混合蒸发可制得乌洛托品,该反应的化学方程式 ;
(5)写出满足下列条件的A的同分异构体
Ⅰ.有两个取代基; Ⅱ.取代基在邻位。
(6)已知:![]() 。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸
。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸 的合成路线流程图(无机试剂可以任选):
的合成路线流程图(无机试剂可以任选):
CH3CH2CHO→ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有0.27kg质量分数为10%的CuCl2溶液。试计算:
(1)溶液中CuCl2的物质的量_______;
(2)溶液中Cu2+和Cl-的物质的量_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com